
| A、0.6 mol/L |
| B、0.8 mol/L |
| C、1.0 mol/L |
| D、1.2 mol/L |
科目:高中化学 来源: 题型:
 CaC2晶体的晶胞结构与NaCl的相似(如图),但CaC2晶体中含有哑铃形C22-的存在,使晶胞沿一个方向拉长.下列关于CaC2晶体的说法中正确的是( )
CaC2晶体的晶胞结构与NaCl的相似(如图),但CaC2晶体中含有哑铃形C22-的存在,使晶胞沿一个方向拉长.下列关于CaC2晶体的说法中正确的是( )| A、6.4克CaC2晶体中含阴离子0.2 mol |
| B、该晶体中的阴离子与N2是互为等电子体 |
| C、1个Ca2+周围距离最近且等距离的C22-数目为6 |
| D、与每个Ca2+距离相等且最近的Ca2+共有12个 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、不同条件下,1mol任何气体所含分子个数均相同 |
| B、1mol任何气体的体积均为22.4L |
| C、1mol气体在压强一定时,50℃时体积比20℃时体积大 |
| D、1LO2和1LO3在同温同压下具有相同数目的分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铝粉投入到NaOH溶液中:2Al+2OH-=2AlO2-+H2↑ |
| B、Fe跟稀盐酸反应:2Fe+6H+=2Fe3++3H2↑ |
| C、金属钾投入到硫酸铜溶液中:2K+Cu2+=2K++Cu |
| D、铜跟稀硝酸反应:3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
 过二硫酸的化学式为H2S2O8,硫元素的形式氧化态可看作是+7,所以是一种强氧化剂.工业上常用电解硫酸和硫酸钾的混合溶液制过二硫酸钾,且在65℃时熔化并分解.电解反应的离子方程式是:2HSO
过二硫酸的化学式为H2S2O8,硫元素的形式氧化态可看作是+7,所以是一种强氧化剂.工业上常用电解硫酸和硫酸钾的混合溶液制过二硫酸钾,且在65℃时熔化并分解.电解反应的离子方程式是:2HSO- 4 |
| ||
2- 8 |
查看答案和解析>>
科目:高中化学 来源: 题型:
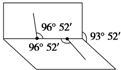 已知H2O2分子的结构如图所示:H2O2分子不是直线形的,两个氢原子犹如在半展开的书的两面上,两个氧原子在书脊位置上,书页夹角为93°52′,而两个O-H键与O-O键的夹角均为96°52′.
已知H2O2分子的结构如图所示:H2O2分子不是直线形的,两个氢原子犹如在半展开的书的两面上,两个氧原子在书脊位置上,书页夹角为93°52′,而两个O-H键与O-O键的夹角均为96°52′.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com