分析:A.氮气的电子式中,氮原子的1对孤电子对没有画出;
B.氯化氢为共价化合物,不需要标出所带电荷;
C.氯化钠为离子化合物,化学式中存在阴阳离子,需要标出所带电荷;
D.二氧化碳为共价化合物,分子中存在两个碳氧双键.
解答:解:A.氮原子核外含有一对孤电子对没有画出,氮气分子中氮原子之间形成3对共用电子对,氮原子含有1对孤对电子对,电子式为
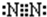
,故A错误;
B.氯化氢为共价化合物,分子中不存在阴阳离子,HCl分子中氢原子与氯原子之间形成1对共用电子对,电子式为
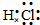
,故B错误;
C.氯化钠为离子化合物,氯离子带电荷并需用方括号括起来,钠离子用离子符号表示,正确的电子式为

,故C错误;
D.二氧化碳为共价化合物,分子中存在两个碳氧双键,二氧化碳的电子式为:
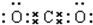
,故D正确;
故选D.
点评:本题考查了电子式的表示方法,题目难度不大,注意明确电子式的概念,掌握离子化合物、共价化合物的电子式的表示方法;选项A为易错点,注意氮气的正确电子式.



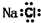
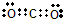
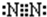 ,故A错误;
,故A错误;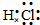 ,故B错误;
,故B错误; ,故C错误;
,故C错误;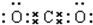 ,故D正确;
,故D正确;

 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案