
| A. | NaHSO4 | B. | KAl(SO4)2 | C. | NaHCO3 | D. | CH3COONa |
分析 依据常温下水的电离平衡影响因素分析,加热促进水的电离,氢离子浓度增大;酸、碱抑制水的电离;水解的盐促进水的电离.
解答 解:A、NaHSO4=Na++H++SO42-;溶液中的氢离子对水的电离起到抑制作用,故A不符合;
B、KAl(SO4)2=K++Al3++2SO42-,溶液中铝离子水解促进水的电离,Al3++3H2O?Al(OH)3+3H+,溶液呈酸性c(H+)增大,故B符合;
C、NaHCO3=Na++HCO3-,溶液中HCO3-水解促进水的电离,HCO3-+H2O?H2CO3+OH-,溶液呈碱性,c(H+)减小,故C不符合;
D、CH3COONa=Na++CH3COO-,溶液中CH3COO-离子水解促进水的电离,CH3COO-+H2O?CH3COOH+OH-,溶液呈碱性,c(H+)减小,故D不符合;
故选B.
点评 本题考查了影响水的电离的因素分析,关键是酸碱抑制水的电离,能水解的盐促进水的电离,题目较简单.


 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:解答题
 ,常用于汽水、糖果的添加剂.
,常用于汽水、糖果的添加剂.查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠的硬度大于铝 | B. | 镁的熔沸点高于钙 | ||
| C. | 镁的硬度大于钾 | D. | 钙的熔沸点高于钾 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 戊二醛分子式为C5H10O2,符合此分子式的二元醛有4种 | |
| B. | 戊二醛不能在加热条件下和新制备的氢氧化铜反应 | |
| C. | 戊二醛不能使酸性KMnO4溶液褪色 | |
| D. | 对有机物分子红外光谱图的研究有助于确定有机物分子中的基团 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 液氨汽化吸收大量的热,可用作制冷剂 | |
| B. | SO2具有还原性,可用作漂白剂 | |
| C. | 晶体硅熔点高硬度大,可用于制作半导体材料 | |
| D. | 常温下浓硫酸具有强氧化性,可用作脱水剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2SiO3与SO2 | B. | Al2(SO4)3和 氨水 | C. | FeI2与Cl2 | D. | NaHCO3与Ca(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
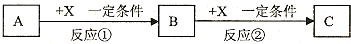
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com