
| A、c(H+) | ||
| B、K(HF) | ||
C、
| ||
D、
|
| c(F-)×c(H+) |
| c(HF) |
| c(H+) |
| c(HF) |
| c(F-)×c(H+) |
| c(HF) |
| c(H+) |
| c(HF) |


科目:高中化学 来源: 题型:
| A、(CH3)2CHCOOC(CH3)3 |
| B、(CH3)2CHCOOCH2CH(CH3)2 |
| C、(CH3)2CHCOOCH(CH3)CH2CH3 |
| D、CH3(CH2)2COOCH2(CH2)2CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 10 |
| A、①②④正确 | B、①③正确 |
| C、②④正确 | D、只有①正确 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| Fe |
| HCl |

 的所有原子
的所有原子查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
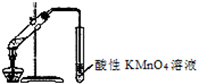 下列实验操作或实验方案设计正确的有.( )
下列实验操作或实验方案设计正确的有.( )| A、②④⑤ | B、①③⑥ |
| C、①③ | D、②④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、亚硝酸钠是常用的防腐剂 |
| B、婴儿食品可添加着色剂,以增加婴儿对食物的兴趣 |
| C、维生素C可防治坏血病,因而我们需要大量补充维生素C |
| D、药物可以帮助我们战胜疾病,但我们仍需合理用药 |
查看答案和解析>>
科目:高中化学 来源: 题型:
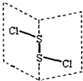 二氯化硫(S2Cl2)广泛用于橡胶工业,分子结构如图.常温下,S2Cl2是一种橙黄色液体,与水迅速反应,并生成能使品红褪色的气体.下列说法正确的是( )
二氯化硫(S2Cl2)广泛用于橡胶工业,分子结构如图.常温下,S2Cl2是一种橙黄色液体,与水迅速反应,并生成能使品红褪色的气体.下列说法正确的是( )A、S2Cl2的电子式: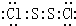 |
| B、S2Cl2为含有极性键和非极性键的非极性分子 |
| C、S2Br2与S2Cl2结构相似,熔沸点:S2Br2<S2Cl2 |
| D、S2Cl2与H2O反应化学方程式可能为:2 S2Cl2+2H2O=SO2↑+3S↓+4HCl |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com