
ʵ������Ҫ 0.1mol/L�� H2SO4��Һ980mL������ 98%���ܶ�Ϊ1.84g/cm3��Ũ��������.
��1���������Ҫ��������Ͳ���ձ����������⣬����Ҫ �� ��
��2����ʵ���������ɷ�Ϊ���¼�����
A������Ͳ��ȡ mLŨ����,����ע��װ��Լ50mL����ˮ���ձ�����ò��������衣
B������������ˮ������ϴ���ձ��Ͳ���������ÿ�ε�ϴҺ����������ƿ�
C����ϡ�ͺ������С�ĵ��ò�������������ƿ�
D���������ƿ�Ƿ�©ˮ��
E��������ˮֱ�Ӽ�������ƿ����Һ��ӽ��̶���1-2cm����
F���ǽ�ƿ���������ߵ���ҡ����Һ��
G���ý�ͷ�ι�������ƿ����μ�������ˮ����Һ����͵�ǡ����������С�
��ݴ���д��
��������������еĿհ״���
�ڲ��������ȷ�IJ���˳������ĸ��д����
�� D ������ A ������ C ������ ������ ������ ������ F ����
�۽�Ũ�������ձ���ϡ�ͺ���������ƿʱ������_________________������Һ.
��3���Է������в�����������Һ��Ũ���к�Ӱ��
����ȡŨ����ʱ�۾�������Ͳ�̶��ߣ��ᵼ��������ҺŨ�Ȼ� ����� ƫ�ߡ�ƫ�͡�����Ӱ�죬��ͬ��
�ڶ���ʱ���۾����ӿ̶��ߣ�������ҺŨ�Ȼ� ��
��1��1000mL����ƿ����ͷ�ι� ��2����5��4mL
�ڣ� B ������ E ������ G �� ����ȴ������ ��3����ƫ�ͣ���ƫ��
��������
�����������1����Ũ����ϡ������ϡ��Һ����Ҫ����������Ͳ���ձ�����������1000mL����ƿ����ͷ�ιܣ���2��������980mL��Һ��Ҫ1000mL������ƿ����ϡ��ǰ�����ʵ��������䣬v��1.84��98%=1L��0.1mol/L��98g/mol������5.4mL���ڲ���ټ������ȡ��ϡ�͢�ת�Ƣ�ϴ�Ӣ��ݡ�ҡ�ȣ�������ƿ������������ʹ�ã�������ȴ�����·�����Һ����3������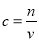 ����ȡŨ����ʱ�۾�������Ͳ�̶��ߣ�ʹn��С����C��С������ʱ���۾����ӿ̶��ߣ�ʹv����C��С��
����ȡŨ����ʱ�۾�������Ͳ�̶��ߣ�ʹn��С����C��С������ʱ���۾����ӿ̶��ߣ�ʹv����C��С��
���㣺���⿼����Һ���ơ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ���Ĵ�ʡ�߶��������л�ѧ�Ծ��������棩 ���ͣ�ѡ����
�±�ΪԪ�����ڱ�ǰ�����ڵ�һ���֣������й�R��W��X��Y��Z����Ԫ�ص������У���ȷ����

A����ѹ������Ԫ�صĵ����У�Z���ʵķе����
B��Y��Z�������ӵ��Ӳ�ṹ����Rԭ�ӵ���ͬ
C��W���⻯��ķе��X���⻯��ķе��
D��YԪ�صķǽ����Ա�WԪ�صķǽ�����ǿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ������ʡ�߶���ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ������
(14��)
��������Ԫ�أ�����A��B��C��DΪ����������Ԫ�أ�E��FΪ��������Ԫ�أ����ǵ�ԭ����������������������������Ϣ���ش����⡣
AԪ��ԭ�ӵĺ���p����������s����������1 |
BԪ��ԭ�Ӻ���s����������p����������ȣ��Ҳ���AԪ����ͬһ���� |
Cԭ�Ӻ�������p���ȫ������� |
DԪ�ص������������������IJ�Ϊ4 |
E��ǰ�������е縺����С��Ԫ�� |
F�����ڱ��ĵ����� |
��1��A��̬ԭ����������ߵĵ��ӣ���������ڿռ��� ������ԭ�ӹ���� �Ρ�
��2��ijͬѧ����������Ϣ��������B�����Ų�ͼ��ͼ
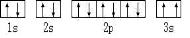
Υ���� ԭ����
��3��Fλ�� �� �������̬ԭ���� ���˶�״̬��
��4��CD3 ����ԭ�ӵ��ӻ���ʽΪ ���ü۲���ӶԻ��������Ʋ�����ӿռ乹��Ϊ ��
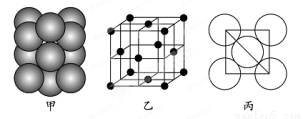
��5����ij�������ʾ�����ԭ�ӵĶѻ���ʽ����ͼ����ʾ���侧����������ͼ����ʾ��ԭ��֮���λ�ù�ϵ��ƽ��ͼ����ͼ����ʾ�����и�ԭ�ӵ���λ��Ϊ ���õ��ʾ�����ԭ�ӵĶѻ���ʽΪ���ֻ����ѻ���ʽ�е� ������֪�ý�����ԭ�Ӱ뾶Ϊd cm��NA���������ӵ����������������ԭ������ΪM����þ�����ܶ�Ϊ______g��cm��3(����ĸ��ʾ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ������ʡ�߶���ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵����ȷ����
A��CHCl3������������
B��H2O��������ԭ��Ϊsp2�ӻ�������Ӽ��ι���ΪV��
C��������̼��̼ԭ��Ϊsp�ӻ���Ϊֱ���η���
D��NH��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ������ʡ�߶���ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����йص����ƺ�ԭ�ӹ����˵����ȷ����
A��ԭ�Ӻ���ĵ���������һ��������ԭ�Ӻ���Χ���ʳƵ�����
B��s�ܼ���ԭ�ӹ�������Σ����ڸù���ϵĵ���ֻ����������˶�
C�����ŵ��Ӳ�����ӣ�p�ܼ�ԭ�ӹ��Ҳ������
D����sԭ�ӹ���ĵ�����ͬ��pԭ�ӹ�����ӵ�ƽ���������ܲ�����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����Ļ�������������һ�и�һ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
���и�����������������Һ�еķ�Ӧ������ͬһ���ӷ���ʽ��ʾ����
A.Ba(OH)2+HCl��KOH+H2SO4
B.KHCO3+HNO3��K2CO3+HNO3
C.NaHCO3+ H2SO4�� Ba(HCO3)2+ H2SO4
D.CuCl2+NaOH��CuSO4+NH3��H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����Ļ�������������һ�и�һ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵����ȷ����
A.����������һ���ǽ�������������������ﲻһ�����Ƿǽ���������
B.����������Ӿ��������Ϊ���������������Ӷ��Ե���
C.�������ǵ���ʵı���������ˮ��Һ�ܷ�
D.���ӷ�Ӧ�Ƿ��ܹ�����Ҫ������֮���ܷ������ֽⷴӦ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����Ļ�������������һ�и߶���ѧ�����л�ѧ�Ծ��������棩 ���ͣ������
��15�֣�
�ں����£��ݻ�Ϊ2L���ܱ������м���1mol N2��X mol H2��������Ӧ:N2��g��+3H2��g�� 2NH3��g����50���ﵽƽ�⣬��÷�Ӧ�ų�������Ϊ18.4 kJ��c��NH3��=0��2mol/L�������ʵ���Ϊ3.6 mol.
2NH3��g����50���ﵽƽ�⣬��÷�Ӧ�ų�������Ϊ18.4 kJ��c��NH3��=0��2mol/L�������ʵ���Ϊ3.6 mol.
��1���÷�Ӧ�Ħ�H= kJ��mol��1
��2���������´˷�Ӧ�Ļ�ѧƽ�ⳣ���ı���ʽK=________________�¶����ߣ���Kֵ________������������С�����䡱����
��3����ʼʱ�����H2�����ʵ���XΪ_____���ӷ�Ӧ��ʼ��ƽ��,��H2��Ũ�ȱ仯��ʾ�ķ�Ӧ����Ϊ��_____________��
��4������ʼʱ����N2 ��H2 ��NH3�����ʵ����ֱ�Ϊa��b��c���ﵽƽ��ʱ����ֵ����ʵ���������ƽ����ͬ��
����ά�ַ�Ӧ����������У�����ʼʱc��ȡֵ��Χ��________________��3�֣�.
����c=2 mol������ͬ�����´ﵽƽ��ʱ���÷�Ӧ���յ�����Ϊ____________ kJ.
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�꽭�ո����и�һ��ѧ�����е��в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���е��뷽��ʽ�У���д��ȷ����
A��Na2SO4=2Na��+SO4��2 B��Ba(OH)2=Ba2++(OH��)2
C��KClO3=K++Cl��+3O2�� D��Fe2(SO4)3��2Fe3��+3SO42��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com