
【题目】实验室测定碳酸钠和碳酸氢钠混合物中碳酸钠的质量分数W(Na2CO3),称取此混合物5.0g,溶于水中,配成250mL溶液.
【方案一】:沉淀法.利用化学反应把HCO3﹣、CO32﹣完全转化为沉淀,称量干燥沉淀的质量,由此计算混合物中ω(Na2CO3).
(1)量取100mL配制好的溶液于烧杯中,滴加足量沉淀剂,把溶液中HCO3﹣、CO32﹣完全转化为沉淀,应选用的试剂是 (填编号).
A.CaCl2溶液 B.MgSO4溶液 C.NaCl溶液 D.Ba(OH)2溶液
(2)将所得沉淀充分干燥,称量沉淀的质量为mg,由此可以计算ω(Na2CO3).如果此步中,沉淀未干燥充分就称量,则测得ω(Na2CO3) (填“偏大”、“偏小“或“无影响”).
【方案二】:量气法.量取10.00mL配制好的溶液与足量稀硫酸溶液反应,测定生成气体在通常状况(约20℃、1.01×105Pa)的体积,由此计算混合物中ω(Na2CO3)。
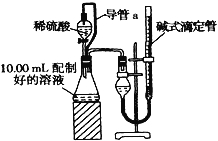
(1)装置中导管a的定量作用是 .
(2)若撤去导管a,使测得气体体积 (“偏大”,“偏小”或“无影响”).
【方案三】:滴定法.量取25.00mL配制好的溶液加入锥形瓶中,滴加2滴酚酞试剂,摇匀,用0.2000molL﹣1的盐酸滴定到终点(已知终点时反应H++CO32﹣═HCO3﹣恰好完全).重复此操作2次,消耗盐酸的体积平均值为20.00mL.
(1)量取25.00mL配制好的溶液,应选择 仪器来完成.
(2)判断滴定终点的依据是 .
(3)此法测得ω(Na2CO3)= %.
【答案】
方案一:(1)D;(2)偏小;
方案二:(1)让锥形瓶中的气体进入分液漏斗上部,保证测量气体体积的准确;(2)偏大;
方案三:(1)碱式滴定管;(2)由红色突变为无色,且30s不恢复;(3)84.8;
【解析】
试题分析:方案一:(1)A.CaCl2溶液只能与碳酸根反应转化为碳酸根沉淀,故A错误;B.MgSO4溶液与HCO3-、CO32-均不反应,故B错误;C.NaCl溶液与HCO3-、CO32-都不反应,故C错误;D.Ba(OH)2溶液与HCO3-、CO32-都发生反应生成碳酸钡沉淀,故D正确;故答案为:D;(2)如果此步中,沉淀未干燥充分就称量,则称量值偏大,由于在质量相等的条件下碳酸氢钠产生的沉淀大于碳酸钠产生的沉淀,所以如果称量值偏大,则碳酸氢钠的质量偏大,则碳酸钠的含量偏小,故答案为:偏小;
方案二:(1)由于碳酸盐与酸反应产生二氧化碳气体,瓶内压强增大,所以装置中导管a的作用是平衡压强、使液体顺利滴下;消除加入稀硫酸引起的体积误差,故答案为:让锥形瓶中的气体进入分液漏斗上部,保证测量气体体积的准确;(2)若撤去导管a会使测得气体体积偏大,故答案为:偏大;
方案三:(1)溶液显碱性,因此应该用碱式滴定管量取,故答案为:碱式滴定管;(2)酚酞的变色范围是8.2~10.0,所以判断滴定终点的依据是由红色突变为无色,且30s不恢复,故答案为:由红色突变为无色,且30s不恢复;(3)反应达到终点时,发生的离子方程式为:H++CO32-=HCO3-,则根据消耗盐酸的体积可知20.00ml可知,消耗碳酸钠的物质的量为:0.2000 mol/L×0.02000L=0.004mol,则原混合物中碳酸钠的物质的量为:0.004mol×![]() =0.04mol,质量为:0.04mol×106g/mol=4.24g,所以碳酸钠质量分数为:
=0.04mol,质量为:0.04mol×106g/mol=4.24g,所以碳酸钠质量分数为:![]() ×100%=84.8%,故答案为:84.8。
×100%=84.8%,故答案为:84.8。


科目:高中化学 来源: 题型:
【题目】某化学研究性学习小组设计了如下图所示的实验装置,目的是做钠与水反应的实脸并验证①钠的物理性质;②钠和水反应的产物。请回答下列问题:

(1)实验开始时,欲使钠与水接触反应,应如何操作?_______________ 。
(2)反应开始后,试管中能观察到的实验现象是:________(填写代号)
A.钠在水层中反应熔成小球并四处游动
B.钠在两液体界面处反应熔成小球并可能作上下跳动
C.钠在水层中反应熔成小球并四处游动
D.钠不断地减小至消失
E.钠停留在煤油层中不反应
F.煤油中有气泡产生
(3)通过上述现象,能够验证钠的哪些物理性质:________________
(4)100 mL 容量瓶中盛有100mL0.101mol/L的BaCl2溶液,现欲将其稀释成浓度为0.100mol/L的BaCl2溶液(体积仍保持为100mL),所选用的仪器有:10mL量筒、1mL移液管(可准确移取0.10~1.00mL溶液)、胶头滴管。其简单的操作步骤是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于热化学方程式书写及对应表达均正确的是 ( )
A.密闭容器中9.6克硫粉与11.2克铁粉混合加热生成硫化亚铁17.6克时放出19.12 kJ热量,则Fe(S)+S(S)=FeS(S) ΔH=-95.6 kJ·mol-1
B.稀醋酸和0.1mol/L的氢氧化钠溶液反应,H+(aq)+OH-(aq) = H2O(l) △H =-57.3kJ/mol
C.已知1 mol氢气完全燃烧生成液态水所放出的热量为285.5 kJ,则水分解的热化学方程式:2H2O(l)=2H2(g)+O2(g) △H = +285.5kJ/mol
D.已知2C(s)+O2(g)=2CO(g) △H=-221 kJ/mol,则可知C的燃烧热△H =-110.5 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】肼(H2N—NH2)是一种高能燃料,有关化学反应的为N2H4(g) + O2 = N2(g) + 2H2O(g) △H=-576 KJ/mol,已知断裂1mol化学键所需的能量(kJ):N≡N为942、O=O为500、N—N为154,H—O为463则断裂1molN—H键所需的能量(kJ)是( )
A.391 B.194 C.516 D.658
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述错误的是
A. 乙烯和苯使溴水褪色的原因不同
B. 苯和氢气在一定条件下生成环己烷的反应为还原反应
C. 硝基苯和乙酸乙酯的制备都发生了取代反应
D. 由乙醇制取乙烯发生了氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在强酸性溶液中能大量共存,并且溶液为无色透明的离子组是( )
A.Ca2+、Na+、NO3﹣、Fe2+
B.Ca2+、Na+、Fe3+、NO3﹣
C.K+、Cl﹣、HCO3﹣、NO3﹣
D.Mg2+、Cl﹣、NH4+、SO42﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组数据中,前者刚好是后者两倍的是
A.2molH2O的摩尔质量和1molH2O的摩尔质量
B.200mL 1mol/L氯化钙溶液中c(Cl-)和100mL 2 mol/L氯化钾溶液中c(Cl-)
C.64gSO2中氧原子数和标准状况下22.4LCO中氧原子数
D.20%NaOH溶液中NaOH的物质的量浓度和10%NaOH溶液中NaOH的物质的量浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在三个密闭容器中分别充入Ne、H2、O2三种气体,当它们的温度和密度都相同时,这三种气体的压强(p)从大到小的顺序是( )
A.p(Ne)>p(H2)>p(O2)
B.p(O2)>p(Ne)>p(H2)
C.p(H2)>p(O2)>p(Ne)
D.p(H2)>p(Ne)>p(O2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在10L恒容密闭容器中充入X(g)和Y(g),发生反应X(g)+Y(g)![]() M(g)+N(g),所得实验数据如下表:
M(g)+N(g),所得实验数据如下表:
实验 编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | |
n(X) | n(Y) | n(M) | ||
① | 700 | 0.40 | 0.10 | 0.090 |
② | 800 | 0.10 | 0.40 | 0.080 |
③ | 800 | 0.20 | 0.30 | a |
④ | 900 | 0.10 | 0.15 | b |
(1) 实验①中,若5min时测得n(M)=0.050mol,则0至5min时间内,用N表示的平均反应速率等于____________。
(2) 实验②中,该反应的平衡常数K=____________。
(3) 实验③中,达到平衡时,X的转化率为____________。
(4) 实验④中,达到平衡时,b____________0.060 (填大于、小于、等于)
(5) 实验③中,达到平衡时,a等于 ____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com