
【题目】下列化学反应的离子方程式正确的是
A. 氢氧化镁中滴加盐酸:H++OH-=H2O
B. 用FeCl3溶液腐蚀铜电路板:Fe3++Cu=Fe2++Cu2+
C. 在硫酸氢钾溶液中加入氢氧化钡溶液至pH=7:H++SO42-+Ba2++OH-=BaSO4↓+H2O
D. NH4HCO3溶液中加入过量NaOH溶液并加热:NH4++HCO3-+2OH-![]() NH3+CO32-+2H2O
NH3+CO32-+2H2O
【答案】D
【解析】
A项,Mg(OH)2难溶于水,应以化学式保留,Mg(OH)2与盐酸反应的离子方程式为:Mg(OH)2+2H+=Mg2++2H2O,A项错误;
B项,电荷不守恒,Cu与FeCl3溶液反应的离子方程式为:Cu+2Fe3+=Cu2++2Fe2+,B项错误;
C项,KHSO4溶液中加入Ba(OH)2溶液至pH=7时化学方程式为:2KHSO4+Ba(OH)2=K2SO4+BaSO4↓+2H2O,离子方程式为:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,C项错误;
D项,NH4HCO3溶液中加入过量NaOH溶液并加热,反应的化学方程式为:NH4HCO3+2NaOH![]() Na2CO3+NH3↑+2H2O,离子方程式为:NH4++HCO3-+2OH-
Na2CO3+NH3↑+2H2O,离子方程式为:NH4++HCO3-+2OH-![]() NH3↑+CO32-+2H2O,D项正确;
NH3↑+CO32-+2H2O,D项正确;
答案选D。


 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案科目:高中化学 来源: 题型:
【题目】某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种。①若加入锌粒,产生无色无味的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示。则下列说法正确的是( )
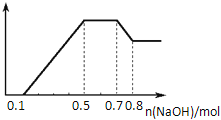
A. 溶液中一定不含CO32﹣,可能含有SO42-和NO3-
B. 溶液中n(NH4+)="0.2" mol
C. 溶液中的阳离子只有H+、Mg2+、Al3+
D. n(H+)︰n(Al3+)︰n(Mg2+)=1︰1︰1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上,可采用还原法处理尾气中NO,其原理:2NO(g)+2H2(g)![]() N2(g)+2H2O(g) △H<0。在化学上,正反应速率方程式表示为v(正)=k(正)·cm(NO)·cn(H2),逆反应速率方程式表示为v(逆)=k(逆)·cx(N2)·cy(H2O),其中,k表示反应速率常数,只与温度有关,m,n,x,y叫反应级数,由实验测定。在恒容密闭容器中充入NO、H2,在T℃下进行实验,测得有关数据如下:
N2(g)+2H2O(g) △H<0。在化学上,正反应速率方程式表示为v(正)=k(正)·cm(NO)·cn(H2),逆反应速率方程式表示为v(逆)=k(逆)·cx(N2)·cy(H2O),其中,k表示反应速率常数,只与温度有关,m,n,x,y叫反应级数,由实验测定。在恒容密闭容器中充入NO、H2,在T℃下进行实验,测得有关数据如下:
实验 | c(NO)/mol·L-1 | c(H2)/mol·L-1 | v(正)/mol·L-1·min-1 |
① | 0.10 | 0.10 | 0.414k |
② | 0.10 | 0.40 | 1.656k |
③ | 0.20 | 0.10 | 1.656k |
下列有关推断正确的是
A. 上述反应中,正反应活化能大于逆反应活化能
B. 若升高温度,则k(正)增大,k(逆)减小
C. 在上述反应中,反应级数:m=2,n=1
D. 在一定温度下,NO、H2的浓度对正反应速率影响程度相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国科学院科研团队研究表明,在常温常压和可见光下,基于 LDH(一种固体催化剂) 合成 NH3 的原理示意图,化学方程式为 2N2+6H2O=4NH3+3O2。下列说法不正确的是()

A. 该过程将太阳能转化成为化学能
B. 该过程中,只涉及共价键的断裂与生成
C. 氧化产物与还原产物的物质的量之比为 4∶3
D. 2molN2 与足量水充分反应,能制得氨气 4mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“生活无处不化学”,请你回答下列问题。
(1)食盐不慎洒落在天然气的火焰上,观察到现象是______,该变化称为______反应。
(2)沾有水的铁制器皿在高温火焰上会发黑,该反应的化学方程式是_______。
(3)小苏打(碳酸氢钠)可用于中和过多的胃酸,写出该反应的离子方程式______。
(4)使用“84”消毒液(含 NaClO)时,按一定比例与水混合,并在空气中浸泡一段时间,使 NaClO 与H2O及空气中的CO2充分 反应,目的是得到杀菌消毒效果更好的______(填物质名称),该反应的离子方程式:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将Mg、Al、Zn组成的混合物与足量的盐酸作用,放出H2的体积为2.8L(标准状况下),则这三种金属的物质的量之和可能为
A. 0.250mol B. 0.100mol C. 0.125mol D. 0.080mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用废旧锂离子电池的正极材料,主要成分为 LiCoO2(难溶于水)还含有 Al以及少量 Ca、Mg、Cu、Fe 等。制备 Co3O4 微球的工艺流程如下:
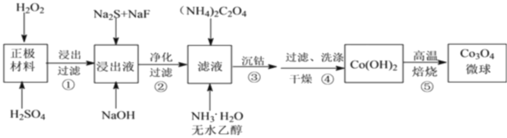
回答下列问题:
(1)LiCoO2 中 Co 元素的化合价为______。
(2)配平步骤①中生成 Co2+的离子方程式为_____LiCoO2 +____H++_____H2 O2 =_____Co2++_____O2 ![]() +_____Li++_____H 2O此过程中若用浓盐酸代替 H2SO4 和 H2O2的混合溶液,除因挥发使其利用率降低外,还有的缺点是_____。
+_____Li++_____H 2O此过程中若用浓盐酸代替 H2SO4 和 H2O2的混合溶液,除因挥发使其利用率降低外,还有的缺点是_____。
(3)步骤②中,不同 pH 下溶液中金属离子的去除效果如下图所示。该过程加入NaOH调节溶液 pH 的最佳范围是______,理由是______。

(4)步骤④中,过滤、洗涤操作均需用到的玻璃仪器有烧杯、玻璃棒、_____。
(5)步骤⑤中,Co(OH)2 在空气中高温焙烧生成 Co3O4 的化学方程式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)工业上氨气的催化氧化反应的化学方程式_____________
(2)偏铝酸钠溶液中通入过量二氧化碳的离子方程式_____________;
(3)根据部分键能数据,以及热化学方程式CH4(g)+4F2(g) = CF4(g)+4HF(g)
ΔH =-1940 kJ·mol-1,计算H—F键的键能为______________。
化学键 | C—H | C—F | H—F | F—F |
键能/(kJ·mol-1) | 414 | 489 | ? | 155 |
(4)0.1mol的氯气和焦炭、TiO2固体完全反应,生成TiCl4液体和一种还原性的气体,放出热量4.28kJ,写出该反应的热化学方程式_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com