
| A. | 明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化 | |
| B. | 在海轮外壳上镶入锌块,可减缓船体的腐蚀速率 | |
| C. | Al2O3的熔点很高,可用于制作耐高温材料 | |
| D. | 电解MgCl2饱和溶液,可制得金属镁 |
分析 A、利用胶体具有大的表面积,有吸附作用分析;
B.锌、铁和海水符合原电池构成条件,能形成原电池;
C.根据氧化铝的物理性质来分析其应用;
D.根据电解氯化镁溶液的反应原理及其产物来判断;
解答 解:A、明矾水解形成的Al(OH)3胶体具有较大的表面积能吸附水中悬浮物,可用于水的净化,故A正确;
B.锌、铁和海水符合原电池构成条件,能形成原电池,锌做负极,铁被保护,可减缓船体的腐蚀速率,故B正确;
C.氧化铝的熔点很高,可用于制作耐高温材料,故C正确;
D.电解MgCl2饱和溶液,发生的化学反应为:MgCl2+2H2O$\frac{\underline{\;通电\;}}{\;}$Mg(OH)2↓+H2↑+Cl2↑,不会产生金属镁,电解熔融的MgCl2能制取单质镁,发生的反应MgCl2Mg+Cl2↑,故D错误;
故选D.
点评 本题考查了盐类水解、金属的冶炼、化合物的性质、原电池的原理应用等知识点,掌握基础是解题关键,题目较简单.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
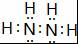 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 6.4g 铜与S完全反应,电子转移0.1 NA个 | |
| B. | 标准状况下,2.24 L水中含有0.1 NA个水分子 | |
| C. | 1.12 L氯气中含有0.1 NA个氯原子 | |
| D. | 0.3molNO2与H2O反应转移的电子数为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
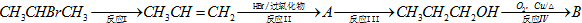 请回答下列问题:
请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 利用与氢气的加成反应除去乙烷中的乙烯得到纯净的乙烷 | |
| B. | 利用溴水鉴别苯和甲苯 | |
| C. | 利用酸性高锰酸钾溶液鉴别乙苯和苯乙烯 | |
| D. | 利用四氯化碳萃取溴水中的溴 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 除去乙烷中的少量乙烯:催化剂和加热条件下通入足量的H2 | |
| B. | 除去乙醇中少量的水:加新制生石灰,蒸馏 | |
| C. | 除去溴苯中少量苯:分液 | |
| D. | 除去硝基苯中的HNO3和H2SO4:加入足量NaOH溶液分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com