
【题目】绿矾是含有一定量结晶水的硫酸亚铁(FeSO4·XH2O),在工农业生产中具有重要的用途。某化学兴趣小组对绿矾的一些性质进行探究。回答下列问题:
(1)在试管中加入少量绿矾样品,加水溶解,滴加KSCN溶液,溶液颜色无明显变化。再向试管中通入空气,溶液逐渐变红。由此可知:______________、_______________;写出相关化学离子方程式:_____________、______________。
(2)为测定绿矾中结晶水含量,将石英玻璃管(带端开关K1和K2)(设为装置A)称重,记为m1 g。将样品装入石英玻璃管中,再次将装置A称重,记为 m2 g。按下图连接好装置进行实验。
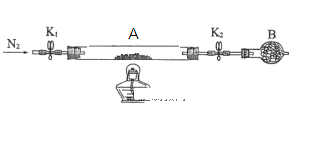
①仪器B的名称是____________________。
②将下列实验操作步骤正确排序___________________(填标号);重复上述操作步骤,直至A恒重,记为m3 g。
a.点燃酒精灯,加热 b.熄灭酒精灯 c.关闭K1和K2
d.打开K1和K2,缓缓通入N2 e.称量A f.冷却至室温
③根据实验记录,计算绿矾化学式中结晶水数目x=________________(列式表示)。若实验时按a、d次序操作,则使x__________(填“偏大”“偏小”或“无影响”)。
(3)为探究硫酸亚铁的分解产物,将(2)中已恒重的装置A接入下图所示的装置中,打开K1和K2,缓缓通入N2,加热。实验后反应管中残留固体为红色粉末。
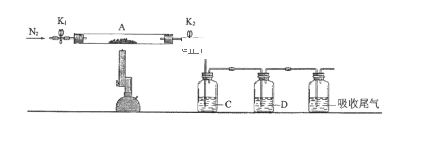
C、D中的溶液依次为BaCl2溶液、浓H2SO4。C、D中有气泡冒出,并可观察到的现象分别为产生白色沉淀、品红溶液褪色。写出硫酸亚铁高温分解反应的化学方程式:_________________________________ 。
【答案】样品中无Fe3+硫酸亚铁易被空气氧化为硫酸铁4Fe2+ +O2 + 4H+ = 4Fe3+ + 2H2OFe3++ 3SCN- = Fe(SCN)3干燥管dabfce![]() 偏小2FeSO4
偏小2FeSO4![]() Fe2O3+SO2↑+SO3
Fe2O3+SO2↑+SO3
【解析】
(1)滴加KSCN溶液,溶液颜色无明显变化,可知样品中无Fe3+,但亚铁离子不稳定,易被空气中氧气氧化生成铁离子,最终溶液变红色,故答案为:样品中无Fe3+;硫酸亚铁易被空气氧化为硫酸铁;4Fe2+ +O2 + 4H+ = 4Fe3+ + 2H2O\Fe3++ 3SCN- = Fe(SCN)3;
(2)①由仪器的图形可知B为干燥管,故答案为:干燥管;
②实验时,为避免亚铁被氧化,应先通入氮气,冷却时注意关闭开关,防止氧气进入,冷却至室温再称量固体质量的变化,则正确的顺序为dabcfe,故答案为:dabcfe;
③直至A恒重,记为m3g,应为FeSO4和装置的质量,则m(FeSO4)=(m3-m1),m(H2O)=(m2-m3),则n(H2O)=![]() mol 、n(FeSO4)=
mol 、n(FeSO4)=![]() mol ,结晶水的数目等于
mol ,结晶水的数目等于![]() =
=![]() ,若实验时按a、d次序操作,会导致硫酸亚铁被氧化,则导致固体质量偏大,测定结果偏小,故答案为:
,若实验时按a、d次序操作,会导致硫酸亚铁被氧化,则导致固体质量偏大,测定结果偏小,故答案为:![]() ;偏小;
;偏小;
(3)①实验后反应管中残留固体为红色粉末,说明生成Fe2O3;C中观察到产生白色沉淀,说明生成了SO3;D中品红褪色,说明生成了SO2,则反应的方程式为:2FeSO4![]() Fe2O3+SO2↑+SO3↑。
Fe2O3+SO2↑+SO3↑。


 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案科目:高中化学 来源: 题型:
【题目】将某铁铝合金样品均分为两份,一份加入足量盐酸,另一份加入足量NaOH溶液,同温同压下产生的气体体积比为3∶2,则样品中铁、铝的物质的量之比为( )
A. 3∶2 B. 2∶1 C. 3∶4 D. 4∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列所示装置正确且能完成相关实验的是( )
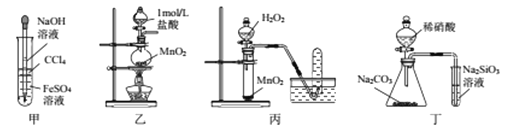
A. 用甲所示装置制取并观察Fe(OH)2 B. 用乙所示装置制取少量Cl2
C. 用丙所示装置制取O2 D. 用丁所示装置比较N、C、Si的非金属性强弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W四种元素在元素周期表中序数逐渐增大。X为非金属元素,且X、W同主族,Y、Z为同周期的相邻元素。W原子的质子数等于Y、Z原子最外层电子数之和。Y的氢化物分子中有3个共价键。Z原子最外层电子数是次外层电子数的3倍。试推断:
(1)X、Y、Z的元素符号分别是:______、_______、________。
(2)画出Z的离子结构示意图__________。
(3)X、Y、Z的简单离子半径大小顺序为________________________________。
(4)用电子式表示W与Z形成化合物W2Z的过程____________________________。
(5)由X、Y、Z所形成的离子化合物是__________,它与W的最高价氧化物对应水化物的溶液加热时反应的离子方程式是________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】肉桂醛F (![]() )在自然界存在于桂油中,是一种常用的植物调味油,工业上主要是按如下路线合成的:
)在自然界存在于桂油中,是一种常用的植物调味油,工业上主要是按如下路线合成的:
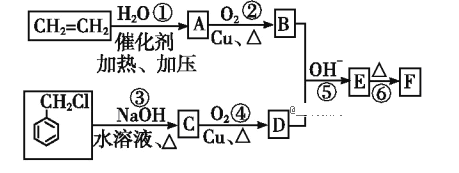
已知:两个醛分子在NaOH溶液作用下可以发生反应,生成一种羟基醛:
![]() +
+ ![]()
![]()
![]()
请回答:
(1)D的名称为__________________。
(2)反应①~⑥中属于加成反应的是___________(填序号)。
(3)写出反应③的化学方程式:______________________________________;
反应④的化学方程式:_________________________________________。
(4)在实验室里鉴定![]() 分子中的氯元素时,是将其中的氯元素转化为AgCl白色沉淀来进行的,其正确的操作步骤是__________(请按实验步骤操作的先后次序填写序号)。
分子中的氯元素时,是将其中的氯元素转化为AgCl白色沉淀来进行的,其正确的操作步骤是__________(请按实验步骤操作的先后次序填写序号)。
A.滴加AgNO3溶液 B.加NaOH溶液 C.加热 D.用稀硝酸酸化
(5)E的同分异构体有多种,其中之一甲属于酯类。甲可由H(已知H的相对分子量为32)和芳香酸G制得,则甲的结构共有__________种。
(6)根据已有知识并结合相关信息日,写出以乙烯为原料制备CH3CH=CHCHO的合成路线流程图(无机试剂任选)。合成路线流程图例如下:_____________________
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
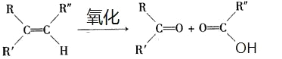
【题目】已知烯烃在酸性KMnO4溶液中双键断裂形式为:

![]()

现有二烯烃C10H18与酸性KMnO4溶液作用后可得到三种有机物:(CH3)2CO、CH3COOH、CH3CO(CH2)2COOH,由此推断此二烯可能的结构简式为
A.(CH3)2C=C(CH3)CH2CH2CH=CHCH2CH3
B.(CH3)2C=CHCH2CH2C(CH3)=CHCH3
C.CH3CH=C(CH3)CH2CH2CH2C(CH3)=CH2
D.CH3CH=C(CH3)CH2CH2CH2CH=CHCH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知: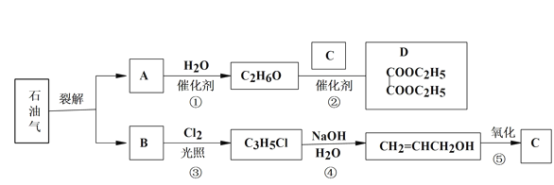
(1)B 和 A 为同系物,B 的结构简式为_____,其含有的官能团名称为_____。
(2)反应①的化学方程式为_____,其反应类型为_____。
(3)写出检验 C3H5Cl 中含有 Cl 原子的方法_____。
(4)C 的结构简式为________。
(5)反应④的化学方程式为________。
(6) 设计一条由乙烯为原料制备 D 的合成路线(其他无机原料任选)。合成路线流程图示例如下:_____
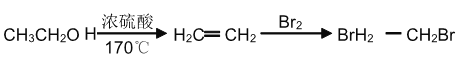
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验小组制备高铁酸钾(K2FeO4)并探究其性质。
资料:K2FeO4为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
(1)制备K2FeO4(夹持装置略)

①A为氯气发生装置。A中反应方程式是___________________________________(锰被还原为Mn2+)。
②将除杂装置B补充完整并标明所用试剂 :______________________________
③C中得到紫色固体和溶液。C中Cl2发生的反应有3Cl2+2Fe(OH)3+10KOH![]() 2K2FeO4+6KCl+8H2O,另外还有____________________________________(写离子方程式)。
2K2FeO4+6KCl+8H2O,另外还有____________________________________(写离子方程式)。
(2)探究K2FeO4的性质
①取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2。为证明是否K2FeO4氧化了Cl-而产生Cl2,设计以下方案:
方案Ⅰ | 取少量a,滴加KSCN溶液至过量,溶液呈红色。 |
方案Ⅱ | 用KOH溶液充分洗涤C中所得固体,再用KOH溶液将K2FeO4溶出,得到紫色溶液b。取少量b,滴加盐酸,有Cl2产生。 |
i.由方案Ⅰ中溶液变红可知a中含有_______离子,但该离子的产生不能判断一定是K2FeO4将Cl-氧化,还可能由__________________________________________产生(用方程式表示)。
ii.方案Ⅱ可证明K2FeO4氧化了Cl-。用KOH溶液洗涤的目的是______________________________。
②根据K2FeO4的制备实验得出:氧化性Cl2_______FeO42-(填“>”或“<”),而方案Ⅱ实验表明,Cl2和FeO42-的氧化性强弱关系相反,原因是________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com