
【题目】居室内空气污染物的主要来源是人们使用的装饰材料、胶黏剂、内墙涂料等释放出来的一种有刺激性气味的气体。据此判断,下列说法不正确的是( )
A. 这种气体是甲醛
B. 这种气体是苯
C. 该气体可用新制氢氧化铜悬浊液进行检验
D. 这种气体可使酸性高锰酸钾溶液褪色
科目:高中化学 来源: 题型:
【题目】(1)N2(g)和H2(g)反应生成1molNH3(g),放出46.1kJ热量,该反应的热化学方程式为____________________________。
(2)已知断裂1mol H2(g)中的H—H键需要吸收436kJ的能量,断裂1mol O2(g)中的共价键需要吸收498kJ的能量,生成H2O(g)中的1mol H—O放出463kKJ的能量。试写出O2(g)与H2(g) 反应生成H2O(g)的热化学方程式____________________________。
(3)发射“神州六号”载人飞船的长征火箭是用肼(N2H4)为燃料,二氧化氮作氧化剂,两者反应生成氮气和水蒸气。已知:N2(g) + 2O2(g) = 2NO2(g)
△H =—67.7 kJ·mol-1;N2H4(g) + O2(g) = N2(g) + 2H2O(g) △H =-534 kJ·mol-1。则肼与二氧化氮反应的热化学方程式为______________________________________。
(4)已知:2H2(g) + O2(g)=2H2O(g) △H=-483kJ·moL-1
N2(g) + 2O2(g)=2NO2(g) △H=+68kJ·moL-1
则H2还原NO2生成水蒸气的热化学方程式是:__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25 ℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
物 质 | X | Y | Z |
初始浓度/ mol·L-1 | 0.1 | 0.2 | 0 |
平衡浓度/ mol·L-1 | 0.05 | 0.05 | 0.1 |
下列说法错误的是
A. 反应达到平衡时,X的转化率为50%
B. 增大压强,使平衡向生成Z的方向移动,平衡常数增大
C. 反应可表示为X+3Y![]() 2Z,其平衡常数为1600
2Z,其平衡常数为1600
D. 改变温度可以改变此反应的平衡常数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积不变的密闭容器中存在如下反应2SO2(g)+O2(g) ![]() 2SO3(g) ΔH<0,某研究小组探究其他条件下不变时,改变某一条件对上述反应的影响,下列分析正确的是
2SO3(g) ΔH<0,某研究小组探究其他条件下不变时,改变某一条件对上述反应的影响,下列分析正确的是
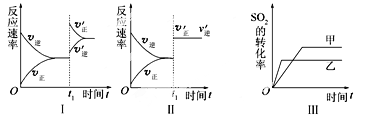
A.图Ⅰ表示的是t1时刻增大O2的浓度对反应速率的影响
B.图Ⅱ表示的是t1时刻加入催化剂后对反应速率的影响
C.图Ⅲ表示的是催化剂对平衡的影响,且甲的催化效率比乙的高
D.图Ⅲ表示的是压强对化学平衡的影响,且乙的压强较高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2 L密闭容器内,800 ℃时反应:2NO(g)+O2(g)![]() 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)(mol) | 0.020 | 0.011 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)写出该反应的平衡常数表达式:K= 。
(2)如图中表示NO2的变化的曲线是 。用O2表示从0~2s内该反应的平均速率v=

(3)能说明该反应已达到平衡状态的是 。
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆 (NO)=2v正 (O2) d.容器内密度保持不变
(4)某同学查阅资料得知,该反应![]() >
>![]() ;25 ℃时,生成1 mol NO2,热量变化为56.4 kJ。但是该同学由于疏忽,忘记注明“+”、“-”。根据题目信息,该反应的热化学方程式为 。
;25 ℃时,生成1 mol NO2,热量变化为56.4 kJ。但是该同学由于疏忽,忘记注明“+”、“-”。根据题目信息,该反应的热化学方程式为 。
(5)为使该反应的反应速率增大,且平衡向正反应方向移动的是 。
a.及时分离除NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,回答下列有关问题:
族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅧA | 0 |
2 | ① | ② | ||||||
3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
4 | ⑩ |
(1)写出下列元素符号:① , ⑥ , ⑦ .
(2)画出原子的结构示意图:④ , ⑧ .
(3)在上述标出元素中,金属性最强的元素是 , 非金属性最强的元素是_ , 最不活泼的元素是 . (均填元素符号
(4)元素⑦与元素⑧相比,非金属性较强的是(用元素符号表示),下列表述中能证明这一事实的是 . (选填序号) a.常温下⑦的单质和⑧的单质状态不同
b.⑧的氢化物比⑦的氢化物稳定
c.一定条件下⑦和⑧的单质都能与氢氧化钠溶液反应
(5)第三周期中原子半径最大的元素是(填元素符号),跟它同周期原子半径(除稀有气体外)最小的元素是(填元素符号)它们最高价氧化物对应水化物之间反应的离子方程式
(6)已知某元素原子最外层电子数是其次外层电子数的2倍,足量该元素的常见氧化物通入③的最高价氧化物的水化物的溶液中,写出化学方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氰(CN)2的结构简式为N≡C—C≡N,其化学性质与卤素(X2)很相似,化学上称之为拟卤素,其氧化性介于Br2和I2之间。下列有关反应的化学方程式不正确的是( )
A. (CN)2+H2=2HCN
B. MnO2+4HCN=Mn(CN)2+(CN)2↑+2H2O
C. 向KCN溶液中加入碘水:I2+2KCN=2KI+(CN)2
D. 在NaBr和KCN混合液中通入少量Cl2:Cl2+2KCN=2KCl+(CN)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以石墨为电极,电解KI溶液(含有少量的酚酞和淀粉).下列说法错误的是
A. 阴极附近溶液显红色 B. 阴极逸出气体
C. 阳极附近溶液呈蓝色 D. 溶液中OH-的物质的量浓度变小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com