
 已知:锂离子电池的总反应为LixC+Li1-xCoO2$?_{充电}^{放电}$C+LiCoO2锂硫电池的总反应为2Li+S$?_{充电}^{放电}$Li2S有关上述两种电池说法正确的是( )
已知:锂离子电池的总反应为LixC+Li1-xCoO2$?_{充电}^{放电}$C+LiCoO2锂硫电池的总反应为2Li+S$?_{充电}^{放电}$Li2S有关上述两种电池说法正确的是( )| A. | 锂离子电池放电时,Li+向负极迁移 | |
| B. | 锂硫电池充电时,锂电极发生氧化反应 | |
| C. | 理论上两种电池的比能量相同 | |
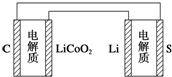
| D. | 下图表示用锂硫电池给锂离子电池充电 |
分析 A.原电池中阳离子向正极移动;
B.锂离子电池放电时,负极发生氧化反应;
C.比能量是参与电极反应的单位质量的电极材料放出电能的大小;
D.给电池充电时,负极与外接电源的负极相连,正极与外接电源的正极相连.
解答 解:A.原电池中阳离子向正极移动,则锂离子电池放电时,Li+向正极迁移,故A错误;
B.锂离子电池放电时,负极发生氧化反应,应失去电子,故B错误;
C.比能量是参与电极反应的单位质量的电极材料放出电能的大小,锂硫电池放电时负极为Li,锂离子电池放电时负极为LixC,两种电池的负极材料不同,所以比能量不同,故C错误;
D.图中表示锂硫电池给锂离子电池充电,右边电极材料是Li和S,锂负极,硫为正极,左边电极材料是C和LiCoO2,由锂离子电池的总反方程式可知C+LiCoO2→LixC+Li1-xCoO2为充电过程即为电解池,则锂硫电池给锂离子电池充电,LiCoO2为阳极失电子发生氧化反应:LiCoO2-xe--xLi+=Li1-xCoO2;C为阴极得电子发生还原反应:C+xe-+xLi+=LixC,则C与负极Li相连,LiCoO2应与正极S相连,故D正确;
故选D.
点评 本题考查了二次电池,为高频考点,侧重于对原电池原理和电解池原理的考查,题目难度中等,注意根据电池总反应判断正负极材料及电极反应.


 学习实践园地系列答案
学习实践园地系列答案科目:高中化学 来源: 题型:解答题
| 滴定次数 | 待测液体积(mL) | 标准KMnO4溶液体积(mL) | |
| 滴定前读数 | 滴定后读数 | ||
| 第一次 | 25.00 | 0.50 | 20.40 |
| 第二次 | 25.00 | 3.00 | 23.00 |
| 第三次 | 25.00 | 4.00 | 24.10 |
| 难溶物 | AgCl | AgBr | AgCN | Ag2CrO4 | AgSCN |
| 颜色 | 白 | 浅黄 | 白 | 砖红 | 白 |
| Ksp | 1.77×10-10 | 5.35×10-13 | 1.21×10-16 | 1.12×10-12 | 1.0×10-12 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸可以用于除去锅炉或水壶中的水垢 | |
| B. | 切开的苹果放置后变色和纸张久置后变黄的原理相同 | |
| C. | 蜂蚁蛰咬人时会向人体注入酸性物质,可涂抹小苏打溶液缓解疼痛 | |
| D. | 工业含酸废水可用氢氧化钡溶液处理后再排放,有利于减少水体污染 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
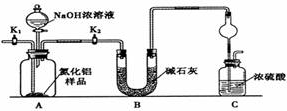
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
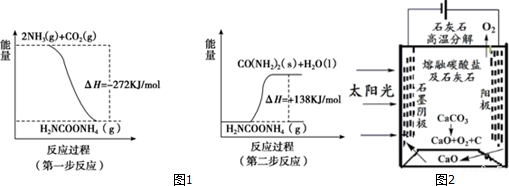
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
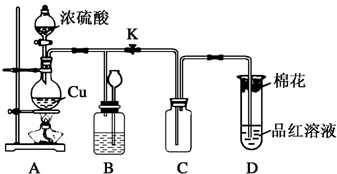
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com