
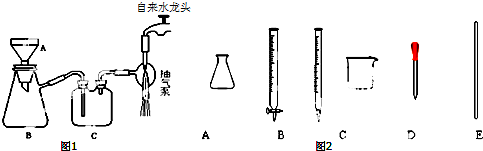
分析 (1)减压的操作优点是:可加快过滤速度,并能得到较干燥的沉淀,所用仪器为布氏漏斗、吸滤瓶、安全瓶、抽气泵,使用时布氏漏斗颈口斜面应与吸滤瓶的支管口相对,且安全瓶中的导气管是短进长出;
(2)高锰酸钾本身有颜色,滴定亚铁离子不需要指示剂,当滴加最后一滴溶液后,溶液变成紫红色,30S内不褪色,说明达到滴定终点;亚铁离子具有还原性,高锰酸根离子具有氧化性,两者发生氧化还原反应;根据滴定操作方法选择使用的仪器.
解答 解:(1)①减压过滤所用仪器为A为布氏漏斗、B为吸滤瓶、C为安全瓶、抽气泵,
故答案为:布氏漏斗;吸滤瓶;
②根据减压过滤装置特点:布氏漏斗颈的斜口要远离且面向吸滤瓶的抽气嘴,并且安全瓶中的导气管是短进长出,所以图中错误为:布氏漏斗颈口斜面应与吸滤瓶的支管口相对;安全瓶的长管和短管连接顺序错误,
故答案为:布氏漏斗颈口斜面应与吸滤瓶的支管口相对;安全瓶的长管和短管连接顺序错误.
(2)①高锰酸钾本身有颜色,滴定亚铁离子不需要指示剂,当滴加最后一滴溶液后,溶液变成紫红色,30S内不褪色,说明达到滴定终点,亚铁离子具有还原性,高锰酸根离子具有氧化性,两者反应为5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O,
故答案为:加入最后一滴KMnO4溶液紫红色不褪,且半分钟内不褪色;5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O;
②滴定操作中需要使用滴定管和锥形瓶,即B、A正确,
故答案为:AB.
点评 本题考查学生常见的化学仪器,要求学生熟悉常见仪器,并掌握其应用,注意掌握过滤、滴定原理是解答本题的关键,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 有些活泼金属如钠、镁、铝可作热还原法的还原剂 | |
| B. | 用电解熔融NaCl的方法来冶炼金属钠 | |
| C. | 回收废旧金属可以重新制成金属或它们的化合物 | |
| D. | 可用焦炭或一氧化碳还原氧化铝的方法来冶炼铝 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
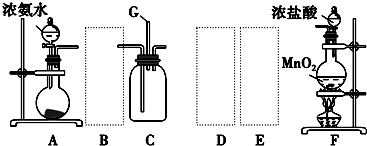
| Ⅰ | Ⅱ | Ⅲ | |
| 备选装置 |  |  | 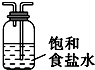 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 哈伯法合成氨是吸热反应,新法合成氨是放热反应 | |
| B. | 新法合成和哈伯法相比不需要在高温条件下,可节约大量能源,具有发展前景 | |
| C. | 新法合成能在常温下进行是因为不需要断裂化学键 | |
| D. | 新的催化剂升高了反应所需要的能量,提高了活化分子百分数 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稀盐酸与稀醋酸的导电性 | |
| B. | 物质的量浓度相等的 (NH4)2Fe(SO4)2溶液和 (NH4)2SO4溶液中NH4+的浓度 | |
| C. | 用量筒量取液体时,仰视的读数和俯视的读数 | |
| D. | 物质的量浓度相等的NaHCO3溶液和Na2CO3溶液中水的电离程度 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 放电时负极反应式为:Zn-2e-+2OH-=Zn(OH)2 | |
| B. | 放电时每转移3mol电子,正极有1 mol K2FeO4被还原 | |
| C. | 充电时阴极附近溶液的碱性增强 | |
| D. | 放电时正极反应式为:Fe(OH)3-3e-+5OH-=FeO42-+4H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解9.6g.向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示(已知硝酸只被还原为NO气体).下列分析或结果错误的是( )
某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解9.6g.向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示(已知硝酸只被还原为NO气体).下列分析或结果错误的是( )| A. | H2SO4浓度为2.5 mol•L-1 | |
| B. | OA段产生的是NO,AB段的反应为Fe+2Fe3+═3Fe2+,BC段产生氢气 | |
| C. | 第二份溶液中最终溶质为FeSO4 | |
| D. | 原混合酸中NO3-物质的量为0.1 mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com