

分析 (1)根据c=$\frac{1000ρω}{M}$计算该浓盐酸中HCl的物质的量浓度;
(2)根据该物理量是否有溶液的体积有关判断;
(3)A.根据容量瓶的使用方法;
B.根据容量瓶用蒸馏水洗净后,再用待配液润洗,待配液中含有溶质;
C.根据容量瓶不能直接用来溶解固体;
D.根据容量瓶不能直接用来稀释溶液;
E.根据定容后,需将溶液摇匀;
(4)①根据溶液稀释定律前后所含溶质的物质的量不变计算;
②分析操作对溶质的物质的量和溶液的体积的影响,依据C=$\frac{n}{V}$进行误差分析.
解答 解:(1)质量分数36.5%,密度为1.19g/mL的盐酸的物质的量浓度=$\frac{1000×1.19×36.5%}{36.5}$=11.9mol/L,
故答案为:11.9;
(2)A.溶液中HCl的物质的量=nV,所以与溶液的体积有关,故A不选;
B.溶液具有均一性,浓度与溶液的体积无关,故B选;
C.溶液的密度与溶液的体积无关,故C选;
D.溶液中Cl-的数目=nNA=CVNA,所以与溶液的体积有关,故D不选;
故选BC;
(3)A.配制溶液时要摇匀,应检验容量瓶是否漏液,故A正确;
B.容量瓶用水洗净后,不能用待配溶液洗涤,否则会引起溶质的物质的量偏多,则所配溶液浓度偏大,故B错误;
C.容量瓶为精密仪器,不能用来溶解固体,故C错误;
D.容量瓶为精密仪器,不能用来稀释浓溶液,故D错误;
E.盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇匀,故E正确;
故选:BCD;
(4)①配制480mL物质的量浓度为0.200mol•L-1的稀盐酸,应选择500mL容量瓶,设需要的浓盐酸的体积为VmL,根据溶液稀释定律C浓V浓=C稀V稀来计算:11.9mol/L×VmL=0.2mol/L×500mL,解得V=8.4mL;
故答案为:8.4;
②A.转移溶液后未洗涤烧杯和玻璃棒就直接定容,导致溶质的物质的量偏小,溶液浓度偏低,故A不选;
B.用量筒量取浓盐酸时俯视观察凹液面,导致量取的氯化氢的物质的量偏小,溶液浓度偏低,故B不选;
C.在容量瓶中定容时俯视刻度线,导致溶液体积偏小,溶液浓度偏高,故C选;
D.定容后把容量瓶倒置摇匀,发现液面低于刻度线,又加水至刻度线,导致溶液体积偏大,溶液浓度偏低,故D不选;
故选:C.
点评 本题考查了一定物质的量浓度溶液的配制过程中的计算和误差分析,侧重考查学生分析实验的能力,明确配制原理是解题关键,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 将钠投入到足量水中 | |
| B. | 将钠用铝箔包好并刺一些小孔,再放入足量水中 | |
| C. | 将钠放入足量稀硫酸中 | |
| D. | 将钠放入足量碳酸氢钠溶液中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子的核外电子数为86 | B. | 中子数为86 | ||
| C. | Rn元素的相对原子量为222 | D. | 质子数为136 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
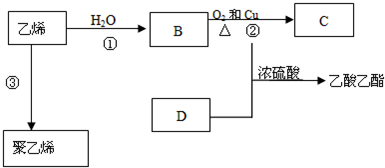
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
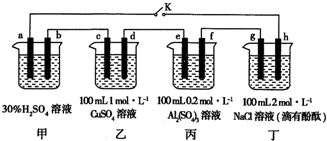
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.7g OH- 所含电子数为0.8NA | |
| B. | 标准状况下,11.2L HCl 所含质子数为18NA | |
| C. | 常温下,11.2L Cl2所含原子数为NA | |
| D. | 0.5mol D2O 中所含质子数为5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3mol NF3与水完全反应生成HF、HNO3和NO,转移电子数2NA | |
| B. | 22.4L CO2与过量的Na2O2反应,转移的电子数为NA | |
| C. | 60 g SiO2晶体中含有2 NA个Si-O键 | |
| D. | 常温下,5.6g铁钉与足量浓硝酸反应,转移的电子数为0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验序号 | 实验现象 | 实验结论 |
| A | 氯水呈浅黄绿色 | 氯水中含有Cl2 |
| B | 向FeCl2溶液中滴加氯水,溶液变成棕黄色 | 氯水中含有HClO |
| C | 向氯水中滴加硝酸酸化的 AgNO3溶液,产生白色沉淀 | 氯水中含有Cl- |
| D | 向氯水中加入NaHCO3粉末,有气泡产生 | 氯水中含有H+ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com