
| A. | 碘单质 | B. | 碘原子 | C. | 碘元素 | D. | 碘离子 |
 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 35.5g | B. | 71g | C. | 119g | D. | 142g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 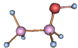 与 与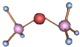 | B. | 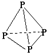 和 和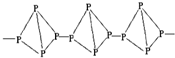 | ||
| C. | ${\;}_{1}^{1}$H2和${\;}_{1}^{2}$H2 | D. | H2O与H2O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
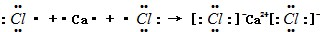 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原白色粉末的组成有3组可能 | |
| B. | 原白色粉末中一定含有CaCO3 | |
| C. | 原白色粉末中一定不含有CuSO4 | |
| D. | 若向无色滤液X中通入二氧化碳,产生白色沉淀,则可推断原白色粉末中一定还含有BaCl2、NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
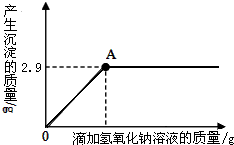 有一不纯的白色固体氯化镁中含有少量氯化钠.化学兴趣小组的同学为了测定该固体氯化镁中氯化钠的质量分数.进行了以下实验:称量10g样品置于烧杯中,向其中加入90g水,搅拌,使其完全溶解为止.然后取该溶液一半,往其中滴加10%的氢氧化钠溶液,产生沉淀的质量与所滴入氢氧化钠溶液的质量关系曲线如图所示.
有一不纯的白色固体氯化镁中含有少量氯化钠.化学兴趣小组的同学为了测定该固体氯化镁中氯化钠的质量分数.进行了以下实验:称量10g样品置于烧杯中,向其中加入90g水,搅拌,使其完全溶解为止.然后取该溶液一半,往其中滴加10%的氢氧化钠溶液,产生沉淀的质量与所滴入氢氧化钠溶液的质量关系曲线如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 ,有机物A的键线式结构为
,有机物A的键线式结构为 ,有机物B与等物质的量的H2发生加成反应可得到有机物,下列有关说法不正确的是( )
,有机物B与等物质的量的H2发生加成反应可得到有机物,下列有关说法不正确的是( )| A. | 用系统命名法命名有机物A,名称为2-甲基戊烷 | |
| B. | 有机物A的一氯取代物有4种 | |
| C. | 有机物A的分子式为C6H14 | |
| D. | B的结构可能有4种 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com