
����Ŀ���ڽӴ���������ͺϳɰ���ҵ�����������У�����˵���������()
A.��������ȼ��ǰҪ���飬Ŀ����ʹ��������ȼ�գ��ӿ췴Ӧ����
B.��������Ĵ�������Ӧ���¶ȿ�����450�����ң���Ҫ���ǵ�����V2O5�Ļ����¶�
C.����������98.3%��Ũ�������ˮ����SO3�������Ч��
D.��ҵ��Ϊ��߷�Ӧ��N2��H2��ת���ʺ�NH3�IJ����ͷ�Ӧ���ʣ����ںϳɰ���Ӧ�ﵽƽ����ٷ��백��
���𰸡�D
��������
A��������ȼ��ǰ��Ҫ�����Ŀ��������Ӧ��ĽӴ�������ӿ췴Ӧ���ʣ�����ȷ��
B����������Ĵ������Ƿ��ȷ�Ӧ�������¶Ȳ���Ϊ���÷�Ӧ�����ƶ��������ǵ�����V2O5�Ļ����¶ȣ���B��ȷ��
C����������SO3�����ˮ���գ�������Ӧ��SO3+H2O![]() H2SO4���÷�ӦΪ���ȷ�Ӧ���ų����������������γɣ���������������ˮ֮�䣬�谭ˮ��������������գ���Ũ����ķе�ߣ����������������γ�������ͬʱ��������������Ũ���ᣬ���Թ�ҵ�ϴ���������������Ũ����������Һ�����յõ������������ᣬ��C��ȷ��
H2SO4���÷�ӦΪ���ȷ�Ӧ���ų����������������γɣ���������������ˮ֮�䣬�谭ˮ��������������գ���Ũ����ķе�ߣ����������������γ�������ͬʱ��������������Ũ���ᣬ���Թ�ҵ�ϴ���������������Ũ����������Һ�����յõ������������ᣬ��C��ȷ��
D���ϳɰ����������н�NH3Һ�����룬����С�����ﰱ����Ũ�ȣ�����ʹ��ѧ��Ӧ���ʼ��������������N2��H2��ת���ʣ���D����
��ѡD��


 A�ӽ��� ϵ�д�
A�ӽ��� ϵ�д� ȫ�Ų��Ծ�ϵ�д�
ȫ�Ų��Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ�����ڣ�����˵������ȷ����![]()
A.��ȿ��������ά��Ҳ����������оƬ
B.����ȿ�����ζ����Ҳ�ɳ�ˮ��
C.���������ȿ�����ȼ����Ҳ������θ�����
D.ʳ�μȿ�����ѩ����Ҳ����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼ��ʾ���ĸ�ԭ���װ�ã����н�����ȷ���ǣ�������
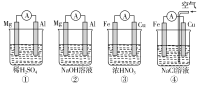
A.�٢���Mg���������ۢ���Fe������
B.����Mg���������缫��ӦʽΪ6H2O��6e��=6OH����3H2��
C.����Fe���������缫��ӦʽΪFe-2e��=Fe2��
D.����Cu���������缫��ӦʽΪ2H����2e��=H2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ũ�Ⱦ�Ϊ0.10mol��L-1�������ΪV0��MOH��ROH��Һ���ֱ��ˮϡ�������V��pH��lg![]() �ı仯��ͼ��ʾ����������������ǣ� ��
�ı仯��ͼ��ʾ����������������ǣ� ��
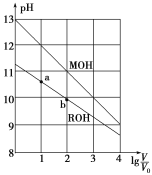
A.MOH�ļ���ǿ��ROH�ļ���
B.ROH�ĵ���̶ȣ�b�����a��
C.������Һ����ϡ�ͣ������ǵ�c(OH-)���
D.��lg![]() =2ʱ��������Һͬʱ�����¶ȣ���
=2ʱ��������Һͬʱ�����¶ȣ���![]() ����
����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����н�����ʵ�Ļ�ѧ��������ȷ����
A.̼�����ϡ���ᷴӦ��CO32+2H+ == H2O+CO2��
B.ͭ��ϡ���ᷴӦ��3Cu+8H++2NO3 == 3Cu2++2NO��+4H2O
C.���Ĵ�������Ӧ��4NH3+5O2 4NO+6H2O
4NO+6H2O
D.������������������������Һ��Ӧ��2OH+SO2== SO32+H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ���������������Ӧ����
A | B | C | D | |
ʵ�� |
|
|
|
|
���� | ������ָ������ƫ��������Feת�Ƶ�Cu����Ƭ�̺�����ƫ | ����һ��ʱ�����Һ��ɫ��ȥ | ���ȣ�����Һ�в�����ɫ���� | �ٺ͢��о�Ѹ�ٲ����������� |
���� | ��Ƭ��������Ƭ�̺�ͭƬ������ | ����������������ˮ�⣬������������ | ������ˮ������Ӧ����H2 | MnO2һ���Ǣ��з�Ӧ�Ĵ��� |
A.AB.BC.CD.D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶��£���2L�����ܱ������г���1molA��1molB��������ӦA(g)+B(g) ![]() C(g)������һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ�IJ������ݼ��±�������˵����ȷ���ǣ��� ��
C(g)������һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ�IJ������ݼ��±�������˵����ȷ���ǣ��� ��
t/s | 0 | 5 | 15 | 25 | 35 |
n(A)/mol | 1.0 | 0.85 | 0.81 | 0.80 | 0.80 |
A.��Ӧ��ǰ5s��ƽ������V(A)=0.03mol/(L��s)
B.���������������䣬�����¶ȣ�ƽ��ʱc(A)=0.41mol��L-1����Ӧ����H>0
C.��ͬ�¶��£���ʼʱ�������г���2.0molC���ﵽƽ��ʱ��C�ķֽ��ʴ���80%
D.��ͬ�¶��£���ʼʱ�������г���0.2molA.0.2molB��1.0molC����Ӧ�ﵽƽ��ǰ��Ӧ����V������<V���棩
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ˮ�д���ƽ��Cl2+H2O![]() HCl+HClO��HClO
HCl+HClO��HClO![]() H++ClO-����ƽ���ҪʹHClOŨ�����ɼ��루 ��
H++ClO-����ƽ���ҪʹHClOŨ�����ɼ��루 ��
A.H2SB.NaHCO3C.����D.NaOH
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com