
”¾ĢāÄæ”æÓĆĻĀĮŠŹµŃé×°ÖĆ½ųŠŠĻąÓ¦ŹµŃ飬ÄÜ“ļµ½ŹµŃéÄæµÄµÄŹĒ£ŗ

A. ÓĆĶ¼(a)ĖłŹ¾×°ÖĆ³żČ„ĀČĘųÖŠŗ¬ÓŠµÄÉŁĮæĀČ»ÆĒā
B. ÓĆĶ¼(d)ĖłŹ¾×°ÖĆ·ÖĄė±½ŻĶČ”µāĖ®ŗóŅŃ·Ö²ćµÄÓŠ»ś²ćŗĶĖ®²ć
C. ÓĆĶ¼(c)ĖłŹ¾×°ÖĆÖĘȔɣĮæ“æ¾»µÄ¶žŃõ»ÆĢ¼ĘųĢå
D. ÓĆĶ¼(b)ĖłŹ¾×°ÖĆÕō·¢ĀČ»ÆÄĘČÜŅŗÖʱøĀČ»ÆÄĘ¾§Ģå
”¾“š°ø”æD
”¾½āĪö”æA£®¶žÕß¾łÓėNaOH·“Ó¦£»
B£®±½µÄĆܶȱČĖ®µÄĆܶȊ”£»
C£®“æ¼īĪŖ·ŪÄ©¹ĢĢ壬²»ÄÜŹµĻÖ¹ĢŅŗ·ÖĄė£»
D£®NaClČÜÓŚĖ®”£
A£®¶žÕß¾łÓėNaOH·“Ó¦£¬Ōņ²»ÄܳżŌÓ£¬Ó¦Ń”±„ŗĶŹ³ŃĪĖ®³żČ„ĀČĘųÖŠŗ¬ÓŠµÄÉŁĮæĀČ»ÆĒā£¬A“ķĪó£»
B£®±½µÄĆܶȱČĖ®µÄĆܶȊ”£¬ŌņĶ¼ÖŠĖ®²ćŌŚĻĀ²ć£¬B“ķĪó£»
C£®“æ¼īĪŖ·ŪÄ©¹ĢĢ壬Ņ×ČÜÓŚĖ®£¬²»ÄÜŹµĻÖ¹ĢŅŗ·ÖĄė£¬²»ÄÜÓĆ¼ņŅ×ĘōĘÕ·¢ÉśĘ÷ÖĘȔɣĮæ“æ¾»µÄ¶žŃõ»ÆĢ¼ĘųĢ壬C“ķĪó£»
D£®NaClČÜÓŚĖ®£¬ŌņÕō·¢ĀČ»ÆÄĘČÜŅŗÖʱøĀČ»ÆÄĘ¾§Ģ壬DÕżČ·£»“š°øŃ”D”£


 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ°“ŅŖĒóĢīæÕ£ŗÓŠĻĀĮŠĪļÖŹ£ŗ¢ŁO2 ¢ŚCO2 ¢ŪNH3 ¢ÜNa2O ¢ŻNa2O2 ¢ŽNaOH ¢ßCaBr2 ¢ąH2O2 ¢įNH4Cl ¢āN2£¬»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)Ö»ŗ¬ÓŠ¼«ŠŌ¼üµÄŹĒ________£»Ö»ŗ¬ÓŠ·Ē¼«ŠŌ¼üµÄŹĒ________£»ŗ¬ÓŠ¼«ŠŌ¼üŗĶ·Ē¼«ŠŌ¼üµÄŹĒ________£»Ö»ŗ¬ÓŠĄė×Ó¼üµÄĄė×Ó»ÆŗĻĪļŹĒ________£»ŗ¬ÓŠ·Ē¼«ŠŌ¼üµÄĄė×Ó»ÆŗĻĪļŹĒ________£»
(2)Š“³ö¢Ż”¢¢ą”¢¢įµÄµē×ÓŹ½_____________”¢______________”¢________________£»
(3)ČÜÓŚĖ®Ö»ĘĘ»µĄė×Ó¼üµÄŹĒ__________£»ČÜÓŚĖ®¼ČĘĘ»µĄė×Ó¼üÓÖĘĘ»µ¹²¼Ū¼üµÄŹĒ________________£»
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æøō¾ųæÕĘų¼ÓČČÖĮ500”ꏱĮņĖįŃĒĢśļ§[(NH4)2Fe(SO4)2]ÄÜĶźČ«·Ö½ā£¬·Ö½ā²śĪļÖŠŗ¬ÓŠĢś Ńõ»ÆĪļ”¢ĮņŃõ»ÆĪļ”¢°±ĘųŗĶĖ®ÕōĘųµČ”£
[ŹµŃéĢ½¾æ]ij»ÆѧŠ”×éŃ”ÓĆĻĀĶ¼ĖłŹ¾²æ·Ö×°ÖĆ½ųŠŠ·Ö²½ŹµŃé(¼Š³Ö×°ÖĆĀŌ)”£
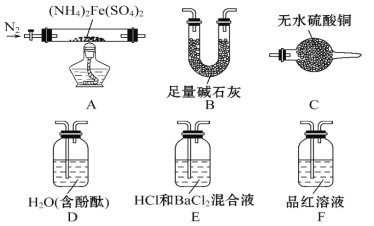
ŹµŃé¢ń ¼×Ķ¬Ń§ĪŖĢ½¾æ·Ö½ā²śĪļÖŠµÄĮņŃõ»ÆĪļŹĒ SO2 »¹ŹĒ SO3£¬Į¬½Ó×°ÖĆA-E-F-B ½ųŠŠŹµŃ锣
(1)ŹµŃé¹ż³ĢÖŠ¹Ū²ģµ½£ŗE ֊ƻӊĆ÷ĻŌĻÖĻó£¬F ÖŠČÜŅŗĶŹÉ«£¬¾Ż“ĖµĆ³öµÄ½įĀŪŹĒ ”£
(2)B µÄ×÷ÓĆŹĒ_____”£
ŹµŃé¢ņ ŃéÖ¤·Ö½ā²śĪļÖŠŗ¬ÓŠĖ®ÕōĘųŗĶ°±Ęų£¬²¢Ģ½¾æ²ŠĮō¹ĢĢå³É·Ö”£
(3)ĖłŃ”ÓĆ×°ÖƵÄÕżČ·Į¬½ÓĖ³ŠņĪŖ_____(Ģī×°ÖƵÄ×ÖÄøŠņŗÅ)”£
(4)Ö¤Ć÷ÓŠĖ®ÕōĘųÉś³ÉµÄŹµŃéĻÖĻóĪŖ_____”£
(5)Ö¤Ć÷ÓŠ°±ĘųÉś³ÉµÄŹµŃéĻÖĻóĪŖ_____”£
(6)A ÖŠ¹ĢĢåĶźČ«·Ö½āŗó±äĪŖŗģ×ŲÉ«·ŪÄ©£¬Éč¼ĘŹµŃéÖ¤Ć÷A ÖŠ²ŠĮō¹ĢĢåÖŠŗ¬ÓŠČż¼ŪĢś_______________”£
(7)ŹµŃéÖ¤Ć÷(NH4)2Fe(SO4)2 ŹÜČČ·Ö½ā³żÉĻŹö²śĪļĶā£¬»¹ÓŠN2 Éś³É£¬Š“³öA ÖŠ·“Ó¦µÄ»Æѧ·½³ĢŹ½__________ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŅĖįŅŅõ„ŹĒŅ»ÖÖÓĆĶ¾¹ć·ŗµÄ¾«Ļø»Æ¹¤²śĘ·”£Ä³æĪĶāŠ”×éÉč¼ĘŹµŃéŹŅÖĘČ”²¢Ģį“æŅŅĖįŅŅõ„µÄ·½°øČēĻĀ£ŗ
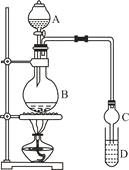
ŅŃÖŖ£ŗ¢ŁĀČ»ÆøĘæÉÓėŅŅ“¼ŠĪ³ÉCaCl2”¤6C2H5OH
¢ŚÓŠ¹ŲÓŠ»śĪļµÄ·Šµć£ŗ
ŹŌ¼Į | ŅŅĆŃ | ŅŅ“¼ | ŅŅĖį | ŅŅĖįŅŅõ„ |
·Šµć/”ę | 34.7 | 78.5 | 118 | 77.1 |
¢Ū2CH3CH2OH![]() CH3CH2OCH2CH3£«H2O
CH3CH2OCH2CH3£«H2O
I£®Öʱø¹ż³Ģ
×°ÖĆČēĶ¼ĖłŹ¾£¬AÖŠ·ÅÓŠÅØĮņĖį£¬BÖŠ·ÅÓŠ9.5mLĪŽĖ®ŅŅ“¼ŗĶ6mL±ł“×Ėį£¬DÖŠ·ÅÓŠ±„ŗĶĢ¼ĖįÄĘČÜŅŗ”£
£Ø1£©Š“³öŅŅĖįÓėŅŅ“¼·¢Éśõ„»Æ·“Ó¦µÄ»Æѧ·½³ĢŹ½ ”£
£Ø2£©ŹµŃé¹ż³ĢÖŠµĪ¼Ó“óŌ¼3mLÅØĮņĖį£¬BµÄČŻ»ż×īŗĻŹŹµÄŹĒ ”””””””” £ØĢīČėÕżČ·Ń”ĻīĒ°µÄ×ÖÄø£©
A£®25mL B£®50mL C£®250mL D£®500mL
£Ø3£©ĒņŠĪøÉŌļ¹ÜµÄÖ÷ŅŖ×÷ÓĆŹĒ ”£
£Ø4£©Ō¤ĻČĻņ±„ŗĶNa2CO3ČÜŅŗÖŠµĪ¼Ó¼øµĪ·ÓĢŖŹŌŅŗ£¬ÄæµÄŹĒ
ӣ
¢ņ£®Ģį“æ·½·Ø£ŗ¢Ł½«DÖŠ»ģŗĻŅŗ×ŖČė·ÖŅŗĀ©¶·½ųŠŠ·ÖŅŗ”£
¢ŚÓŠ»ś²ćÓĆ5mL±„ŗĶŹ³ŃĪĖ®Ļ“µÓ£¬ŌŁÓĆ5mL±„ŗĶĀČ»ÆøĘČÜŅŗĻ“µÓ£¬×īŗóÓĆĖ®Ļ“µÓ”£ÓŠ»ś²ćµ¹ČėŅ»øÉŌļµÄÉÕĘæÖŠ£¬ÓĆĪŽĖ®ĮņĖįĆ¾øÉŌļ£¬µĆ“Ö²śĪļ”£
¢Ū½«“Ö²śĪļÕōĮó£¬ŹÕ¼Æ77.1”ęµÄĮó·Ö£¬µĆµ½“æ¾»øÉŌļµÄŅŅĖįŅŅõ„”£
£Ø5£©µŚ¢Ł²½·ÖŅŗŹ±£¬Ń”ÓƵÄĮ½ÖÖ²£Į§ŅĒĘ÷µÄĆū³Ę·Ö±šŹĒ ”¢ ”£
£Ø6£©µŚ¢Ś²½ÖŠÓƱ„ŗĶŹ³ŃĪĖ®”¢±„ŗĶĀČ»ÆøĘČÜŅŗ”¢×īŗóÓĆĖ®Ļ“µÓ£¬·Ö±šÖ÷ŅŖĻ“Č„“Ö²śĘ·ÖŠµÄ £¬ £¬ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ20”ꏱ£¬ÅäÖĘŅ»×éc(Na2CO3)+c(NaHCO3)=0.100 mol”¤L-1µÄ»ģŗĻČÜŅŗ£¬ČÜŅŗÖŠc(HCO3-)”¢c(CO32-)ÓėpHµÄ¹ŲĻµČēÓŅĶ¼ĖłŹ¾”£ĻĀĮŠÖø¶ØČÜŅŗÖŠĪ¢Į£µÄĪļÖŹµÄĮæÅØ¶Č¹ŲĻµÕżČ·µÄŹĒ

A. pH=9µÄČÜŅŗÖŠ£ŗc(HCO3-)>c(H2CO3)+c(CO32-)
B. c(HCO3-)= c(CO32-)µÄEµćČÜŅŗÖŠ£ŗc(OH-)+c(CO32-)>c(H+)+ c(H2CO3) +0.050 mol”¤L-1
C. pH=11µÄČÜŅŗÖŠ£ŗc(Na+)<2c(CO32-)+c(HCO3-)
D. 0.100 mol”¤L-1µÄNa2CO3ČÜŅŗÖŠ£ŗc(H+)+c(H2CO3) + c(HCO3-)=c(OH-)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖ±½ŅŅĻ©(b)”¢Į¢·½Ķé(d)”¢»·ŠĮĖÄĻ©(p)µÄ·Ö×ÓŹ½¾łĪŖC8H8”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ

A. b”¢dµÄ¶žĀČ“śĪļ¾łÖ»ÓŠČżÖÖ B. b”¢p¾łÄÜÓėĖįŠŌøßĆĢĖį¼ŲČÜŅŗ·“Ó¦
C. dŹĒĶéĢž£¬Ö»ÄÜČ”“ś£¬²»ÄÜ¼Ó³É D. bŗĶ±½ŅŅČ²Ņ»Ńł£¬ĖłÓŠŌ×ÓŅ»¶Ø“¦ÓŚĶ¬Ņ»Ę½Ćę
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ³£ĪĀĻĀ£¬ŌŚŠĀÖĘĀČĖ®ÖŠµĪ¼ÓNaOH ČÜŅŗ,ČÜŅŗÖŠĖ®µēĄė³öĄ“µÄcĖ®(H+)µÄ¶ŌŹżÓėNaOH ČÜŅŗĢå»żÖ®¼äµÄ¹ŲĻµČēĶ¼ĖłŹ¾”£ĻĀĮŠĶʶĻÕżČ·µÄŹĒ

A. ÓĆpHŹŌÖ½²ā¶ØEµć¶ŌÓ¦µÄČÜŅŗ£¬ĘäpH=3
B. F”¢Hµć¶ŌÓ¦µÄČÜŅŗÖŠ¶¼“ęŌŚc(Na+)=c(Cl-)+c(ClO-)
C. Gµć¶ŌÓ¦µÄČÜŅŗÖŠc(Na+)>c(Cl-)>c(ClO-)>c(OH-)>c(H+)
D. ¼ÓĖ®Ļ”ŹĶHµć¶ŌÓ¦µÄČÜŅŗ,ČÜŅŗµÄpHŌö“ó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijæĪĶāŠ”×éŃŠ¾æĀĮĶĮæóÖŠAl2O3µÄŗ¬Į攣²éŌÄ׏ĮĻµĆÖŖ£¬ĀĮĶĮæóµÄÖ÷ŅŖ³É·ÖŹĒAl2O3£¬ŌÓÖŹŹĒFe2O3”¢SiO2µČ”£“ÓĀĮĶĮæóÖŠĢįČ”Al2O3µÄ¹ż³ĢČēĻĀ£ŗ

(1)µŚ¢Ł²½£¬ĻņĀĮĶĮæóÖŠ¼ÓČė×ćĮæÉÕ¼īČÜŅŗ£¬³ä·Ö·“Ó¦£¬·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½ŹĒ£ŗ______________ ”¢________________£»
(2)µŚ¢Ū²½ÖŠ£¬Éś³ÉĒāŃõ»ÆĀĮµÄĄė×Ó·½³ĢŹ½ŹĒ_____________”£ČōĶłAČÜŅŗÖŠĶØČė×ćĮæCO2£¬²śÉśµÄ³ĮµķĪŖ____________________(Ģī»ÆѧŹ½)£»
(3)¹¤ŅµÉĻÖĘČ”AlCl3³£ÓĆAl2O3ÓėC”¢Cl2ŌŚøßĪĀĢõ¼žĻĀ·“Ó¦£¬ŅŃÖŖĆæĻūŗÄ0.5molĢ¼µ„ÖŹ£¬×ŖŅĘ1molµē×Ó£¬ŌņøĆ·“Ó¦µÄŃõ»Æ²śĪļĪŖ_____________(Ģī»ÆѧŹ½)”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æµŖµÄŃõ»ÆĪļŗĶĮņµÄŃõ»ÆĪļŹĒµ¼ÖĀĖįÓźµÄĪļÖŹ”£
(1)SO2ÓŠ¶¾,ĒŅÄÜŠĪ³ÉĖįÓź,ŹĒ“óĘųÖ÷ŅŖĪŪČ¾ĪļÖ®Ņ»”£ŹÆ»Ņ-ŹÆøą·ØŗĶ¼ī·ØŹĒ³£ÓƵÄŃĢĘųĶŃĮņ·Ø”£ŹÆ»Ņ-ŹÆøą·ØµÄĪüŹÕŌĄķ:
¢ŁSO2+Ca(OH)2=CaSO3”ż+H2O¢Ś2CaSO3+O2+4H2O=2(CaSO4”¤2H2O)¼ī·ØµÄĪüŹÕŌĄķ:½«ŗ¬SO2µÄĪ²ĘųĶØČė×ćĮæµÄÉÕ¼īČÜŅŗÖŠ,ĒėŠ“³ö¶ŌÓ¦µÄ»Æѧ·“Ó¦·½³ĢŹ½__________;
ŅŃÖŖ:
ŹŌ¼Į | Ca(OH)2 | NaOH |
¼Ūøń(ŌŖ/kg) | 0.36 | 2.9 |
ŗĶŹÆ»Ņ-ŹÆøą·ØĻą±Č,¼ī·ØµÄÓŵćŹĒĪüŹÕæģ”¢Š§ĀŹøß,ȱµćŹĒ__________;
(2)ŹÆ»Ņ-ŹÆøą·ØŗĶ¼ī·ØµÄ»ł“”ÉĻ,Éč¼ĘĮĖĖ«¼ī·Ø,ÄÜŹµĻÖĪļĮĻŃ»·ĄūÓĆ”£

ÉĻŹö·½·ØÖŠ,ŹµĻÖŃ»·ĄūÓƵÄĪļÖŹŹĒ__________,ĒėÓĆ»Æѧ·½³ĢŹ½±ķŹ¾ŌŚNa2SO3ČÜŅŗÖŠ¼ÓČėCaOŗóµÄ·“Ó¦ŌĄķ__________”£
(3)Ņ»¶ØĢõ¼žĻĀ°±ĘųŅąæÉÓĆĄ“½«µŖŃõ»ÆĪļ×Ŗ»ÆĪŖĪŽĪŪČ¾µÄĪļÖŹ”£Š“³ö°±ĘųŗĶ¶žŃõ»ÆµŖŌŚŅ»¶ØĢõ¼žĻĀ·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ____________
(4)ÓĆĒāŃõ»ÆÄĘČÜŅŗæÉŅŌĪüŹÕ·ĻĘųÖŠµÄµŖŃõ»ÆĪļ£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ČēĻĀ£ŗ
NO2£«NO£«2NaOH£½2NaNO2£«H2O
2NO2£«2NaOH£½NaNO2£«NaNO3£«H2O
ĻÖÓŠVLijNaOHČÜŅŗÄÜĶźČ«ĪüŹÕn mol NO2ŗĶm mol NO×é³ÉµÄ“óĘųĪŪČ¾Īļ”£
¢ŁĖłÓĆÉÕ¼īČÜŅŗµÄĪļÖŹµÄĮæÅضČÖĮÉŁĪŖ________mol”¤L£1”£
¢ŚČōĖłµĆČÜŅŗÖŠc(NO3-)”Ćc(NO2-)£½1”Ć9£¬ŌņŌ»ģŗĻĘųĢåÖŠNO2ŗĶNOµÄĪļÖŹµÄĮæÖ®±Čn”Ćm£½________”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com