
| A. | V>40 | B. | 20<V<40 | C. | V=40 | D. | V=20 |
分析 发生MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,浓盐酸变为稀盐酸后,稀盐酸与二氧化锰不反应,则实际消耗盐酸大于理论计算值,以此来解答.
解答 解:n(Cl2)=$\frac{2.24L}{22.4L/mol}$=0.1mol,由MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O可知,n(HCl)=4n(Cl2)=0.4mol,
则消耗盐酸的体积V′=$\frac{0.4mol}{10mol/L}$=0.04L=40mL,
浓盐酸变为稀盐酸后,稀盐酸与二氧化锰不反应,则实际消耗盐酸大于理论计算值,即V>40,
故选A.
点评 本题考查氧化还原反应的计算,为高频考点,把握发生的反应及物质的量关系为解答的关键,注意稀盐酸与二氧化锰不反应,侧重分析与计算能力的考查,题目难度不大.


科目:高中化学 来源: 题型:解答题

| 物质 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Cu(OH)2 |
| 开始沉淀pH | 2.7 | 7.6 | 8.3 | 4.7 |
| 完全沉淀pH | 3.7 | 9.6 | 9.8 | 6.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


 .
. (其中任一种).
(其中任一种).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 开始滴加氨水时形成的难溶物为Cu(OH)2 | |
| B. | 沉淀溶解后,生成深蓝色的配合离子[Cu(NH3)4]2+配位数为4 | |
| C. | 反应后溶液中不存在任何沉淀,所以反应前后Cu2+的浓度不变 | |
| D. | [Cu(NH3)4]2+中,Cu2+提供空轨道,NH3给出孤电子对 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 相对分子质量相同、结构不同的化合物一定互为同分异构体 | |
| B. | 含不同碳原子数的烷烃一定互为同系物 | |
| C. | 结构对称的烷烃,其一氯取代产物必定只有一种 | |
| D. | 分子通式相同且组成上相差一个或几个CH2原子团的物质互为同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
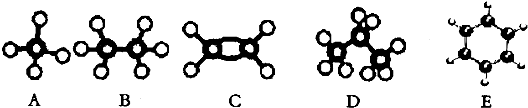
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
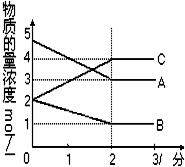 在密闭容器中,某反应在不同反应时间各物质的量的变化情况如图所示
在密闭容器中,某反应在不同反应时间各物质的量的变化情况如图所示 2C.
2C.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com