
在两个密闭容器中,分别充有质量相同的甲、乙两种气体,若它们的温度和密度均相同,试根据甲、乙的摩尔质量(M)关系,判断下列说法正确的是( )
A.若M(甲)>M(乙),则气体体积:甲<乙
B.若M(甲)<M(乙),则气体的压强:甲>乙
C.若M(甲)>M(乙),则气体的摩尔体积:甲<乙
D.若M(甲)<M(乙),则的分子数:甲<乙
B
【解析】
试题分析:A.n=m÷M,由于质量相等,所以若M(甲)>M(乙),则n(甲)>n(乙),由于n=V÷Vm,所以气体体积:甲>乙,错误;B.n=m÷M,由于质量相等,所以若M(甲)<M(乙),则n(甲)>n(乙),由于气体的质量相同、密度均相同所以气体的体积相同,单位体积内气体的物质的量越多,气体的压强就越大。所以气体的压强:甲>乙,正确;C.在相同的外界条件下,不同气体的气体的摩尔体积相同,与气体的种类、摩尔质量无关,错误; D.n=m÷M,由于质量相等,所以若M(甲)<M(乙),则n(甲)>n(乙)。N=n·NA,气体的物质的量越多,气体分子数就越多,所以分子数:甲>乙,错误。
考点:考查阿伏伽德罗定律的应用的知识。


 名题金卷系列答案
名题金卷系列答案科目:高中化学 来源:2015届河北省石家庄市五校联考高三上学期第一次月考化学试卷(解析版) 题型:选择题
(6分)将由 、
、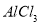 、
、 三种固体组成的 混合物溶于足量水,充分反应后得到
三种固体组成的 混合物溶于足量水,充分反应后得到 白色沉淀,向所得的浊液中逐滴加入
白色沉淀,向所得的浊液中逐滴加入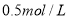 的盐酸,生成沉淀的质量与加入盐酸的体积的关系如图所示:
的盐酸,生成沉淀的质量与加入盐酸的体积的关系如图所示:

求:(1)分别求混合物中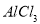 、
、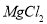 物质的量
物质的量
(2) 点时加入
点时加入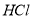 的体积(要求写出计算过程)
的体积(要求写出计算过程)
查看答案和解析>>
科目:高中化学 来源:2015届江西省红色六校高三第一次联考化学试卷(解析版) 题型:填空题
(13分)综合利用CO2对环境保护及能源开发意义重大。
(1)Li2O、Na2O、MgO均能吸收CO2。如果寻找吸收CO2的其他物质,下列建议合理的是 。
A.可在酸性氧化物中寻找 B.可在碱性氧化物中寻找
C.可在ⅠA、ⅡA族元素形成的氧化物中寻找 D.可在具有强氧化性的物质中寻找
(2)Li2O吸收CO2后,产物用于合成Li4SiO4,Li4SiO4用于吸收、释放CO2。原理是:在500℃,CO2与Li4SiO4接触后生成Li2CO3;平衡后加热至700℃,反应逆向进行,放出CO2,Li4SiO4再生,说明该原理的化学方程式是 。
(3)利用反应A可将释放的CO2转化为具有工业利用价值的产品。
反应A: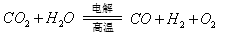 已知:
已知:
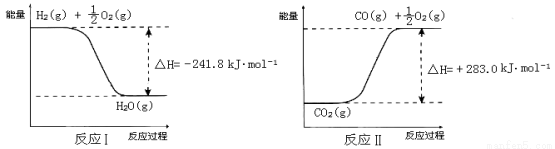
① 反应Ⅱ是_____反应(填“吸热”或“放热”)。
② 反应A的热化学方程式是 。
(4)如图所示装置I是一种可充电电池,装置Ⅱ为电解池。离子交换膜只允许Na+通过,充放电的化学方程式为2Na2S2+NaBr3  Na2S4+3NaBr 闭合开关K时,b极附近先变红色。则
Na2S4+3NaBr 闭合开关K时,b极附近先变红色。则
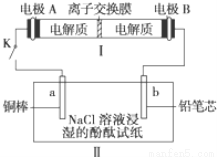
①负极反应式为:
②当有0.02 mol Na+通过离子交换膜时,b电极上析出的气体体积为 mL
③闭合K后,b电极附近的pH (填变大、变小或不变);
同时a电极反应式为
查看答案和解析>>
科目:高中化学 来源:2015届江西省红色六校高三第一次联考化学试卷(解析版) 题型:选择题
以下关于化学实验中“先与后”的说法中正确的是( )
①加热试管时,先均匀加热,后局部加热;
②用排水法收集气体时,先移出导管后撤酒精灯;
③制取物质时,先检查装置气密性后装药品;
④使用容量瓶、分液漏斗、滴定管前,先检查是否漏水后洗涤干净;
⑤做H2还原CuO实验时,先加热CuO后通H2;反应完毕后,先撤酒精灯待试管冷却后停止通H2。
A.除②以外 B.除④以外 C.除⑤以外 D.全部正确
查看答案和解析>>
科目:高中化学 来源:2015届江西省上学期高三第一次月考化学试卷(解析版) 题型:填空题
(6分)(1)向MnSO4和硫酸的混合溶液里加入K2S2O8(过二硫酸钾),溶液会发
如下反应:Mn2++S2O82-+H2O→MnO4-+SO42-+H+该反应常用于检验Mn2+的存在。其特征现象是___________。
若反应中有0.1 mol还原剂参加反应,则消耗氧化剂物质的量__________mol。
(2)若该反应所用的硫酸锰改为氯化锰,当它跟过量的过硫酸钾反应时,除有高锰酸钾、硫酸钾、硫酸生成外,其他的生成物还有_________________。
(3)将NaBiO3固体(黄色微溶)加入到MnSO4和H2SO4的混合溶液里加热,固体溶解变为澄清溶液,发生如下反应: NaBiO3+ MnSO4+ H2SO4— Na2SO4+ Bi2(SO4)3+ NaMnO4+ H2O
①配平上述反应的化学方程式,并标出电子转移的方向和数目;
②上述反应中还原产物是
查看答案和解析>>
科目:高中化学 来源:2015届江西省上学期高三第一次月考化学试卷(解析版) 题型:选择题
16.8gNaHCO3和7.8gNa2O2在密闭容器中灼烧,充分反应后,将密闭容器保持温度为500℃,最后容器内物质是( )
A.Na2CO3,Na2O,O2 B.Na2CO3,CO2,O2,H2O(g)
C.Na2CO3,O2,H2O(g) D.NaHCO3,Na2CO3,O2
查看答案和解析>>
科目:高中化学 来源:2015届江西省高三第二次月考化学试卷(解析版) 题型:填空题
(12分) 铝是重要的金属材料,铝土矿(主要成分是Al2O3和少量的SiO2、Fe2O3杂质)是工业上制取铝的原料。实验室模拟工业上以铝土矿为原料制取Al2(SO4)3和铵明矾晶体[NH4Al(SO4)2·12H2O]的工艺流程如图所示:

请回答下列问题:
(1)固体a的化学式为________,Ⅲ中通入足量CO2气体发生反应的离子方程式为_________________。
(2)由Ⅴ制取铵明矾溶液的化学方程式为 。
从铵明矾溶液中获得铵明矾晶体的实验操作依次为(填操作名称) 、冷却结晶、过滤洗涤。
(3)以1 000 kg含氧化铝36%的铝土矿为原料制取Al2(SO4)3,需消耗质量分数98%的硫酸(密度1.84 g·cm-1) L(计算结果请保留一位小数)。
(4)若同时制取铵明矾和硫酸铝,通过控制硫酸的用量调节两种产品的产量。若欲使制得的铵明矾和硫酸铝的物质的量之比为1∶1,则投料时铝土矿中的Al2O3和H2SO4的物质的量之比为 。
查看答案和解析>>
科目:高中化学 来源:2015届江西省高三第二次月考化学试卷(解析版) 题型:选择题
某溶液中存在XO-,且X为短周期元素,则一定能在该溶液中大量共存的离子组是
A.Na+、H+、SO 、I- B.Na+、Ca2+、CO
、I- B.Na+、Ca2+、CO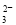 、Al3+
、Al3+
C.Na+、K+、Fe2+、H+ D.K+、SO 、Cl-、CO
、Cl-、CO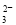
查看答案和解析>>
科目:高中化学 来源:2015届江西省高三上学期第一次月考化学试卷(解析版) 题型:选择题
一种新型镁铝合金的化学式为Mg17Al12,它具有储氢性能,该合金在一定条件下完全吸氢的化学方程式为:Mg17Al12+17H2=17MgH2+12Al,得到的混合物Y(17MgH2+12Al)在一定条件下能释放出氢气。下列说法正确的是
A.该合金的熔点介于金属镁和金属铝熔点之间
B.该合金中镁元素呈负价,铝元素呈正价
C.1mol Mg17Al12完全吸氢后得到的混合物Y与盐酸完全反应释放出H2,若消耗盐酸的体积为14L,则该盐酸的物质的量浓度为5mol.L-1
D.制备该合金应在氮气保护下,将一定比例的Mg、Al单质在一定温度下熔炼而获得
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com