
【题目】实验室制备硝基苯的主要步骤如下:
①配制一定比例的浓H2SO4与浓HNO3的混合酸,加入反应器中;
②向室温下的混合酸中逐滴加入一定量的苯,充分振荡,混合均匀;
③在50~60℃下发生反应,直至反应结束;
④除去混合酸后,粗产品依次用蒸馏水和5% NaOH溶液洗涤,
最后再用蒸馏,水洗涤;
⑤将用无水CaCl2干燥后的粗硝基苯进行蒸馏,得到纯净硝基苯.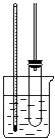
请填写下列空白:
(1)配制一定比例浓H2SO4与浓HNO3混合酸时,如何混合? .
(2)步骤③中,为了使反应在50~60℃下进行,常用的方法是;
(3)装置中常在试管上连接玻璃管,作用是什么? .
(4)步骤④中洗涤、分离粗硝基苯应使用的仪器是 .
(5)步骤④中粗产品用5% NaOH溶液洗涤的目的是 .
【答案】
(1)把浓硫酸慢慢注入浓硝酸中并不断搅拌(或混合放出大量的热,将密度大的注入密度下的溶液中,并不断搅拌)
(2)水浴加热
(3)冷凝兼回流挥发的苯和浓硝酸
(4)分液漏斗
(5)洗去粗产品中的酸性杂质
【解析】解:(1.)类比浓硫酸的稀释可知,配制一定比例浓H2SO4与浓HNO3混合酸的方法为:把浓硫酸慢慢注入浓硝酸中并不断搅拌,所以答案是:把浓硫酸慢慢注入浓硝酸中并不断搅拌(或混合放出大量的热,将密度大的注入密度下的溶液中,并不断搅拌);
(2.)在50℃~60℃下发生反应,温度小于100℃,采取水浴加热,使受热均匀,便于控制温度,所以答案是:水浴加热;
(3.)苯与浓硝酸易挥发,长导管冷凝兼回流挥发的苯和浓硝酸,减少损失,所以答案是:冷凝兼回流挥发的苯和浓硝酸;
(4.)分离互不相溶的液体采用分液方法分离,分液操作使用的仪器是分液漏斗,所以答案是:分液漏斗;
(5.)氢氧化钠溶液具有碱性,能中和未反应的酸,所以氢氧化钠的作用是洗去粗产品中的酸性杂质,所以答案是:洗去粗产品中的酸性杂质.


 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案科目:高中化学 来源: 题型:
【题目】将纯水加热至较高温度,下列叙述正确的是( )
A.水的离子积变大、pH变小、呈酸性
B.水的离了积不变、pH不变、呈中性
C.水的离子积变小、pH变大、呈碱性
D.水的离子积变大、pH变小、呈中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酰氯(SO2Cl2)常作氯化剂或氯璜化剂,用于制作药品、染料、表面活性剂等。有关物质的部分性质如下表:
物质 | 熔点/℃ | 沸点/℃ | 其它性质 |
SO2Cl2 | -54.1 | 69.1 |
②易分解:SO2Cl2 SO2↑+Cl2↑ |
H2SO4 | 10.4 | 338 | 具有吸水性且不易分解 |
实验室用干燥而纯净的二氧化硫和氯气合成硫酰氯,反应的化学方程式为SO2(g)+Cl2(g) ![]() SO2Cl2(l)△H=-97.3kJ/mol。装置如图所示(夹持仪器已省略),请回答有关问题:
SO2Cl2(l)△H=-97.3kJ/mol。装置如图所示(夹持仪器已省略),请回答有关问题:

(1)仪器B的作用是_____________________。
(2)若无装置乙硫酰氯会发生水解,则硫酰氯水解反应的化学方程式为________________。
(3)写出丁装置中发生反应的化学反应方程式并标出电子的转移__________________。
(4)为提高本实验中硫酰氯的产率,在实验操作中需要注意的事项有_________(填序号)
①先通冷凝水,再通气 ②控制气流速率,宜慢不宜快
③若三颈烧瓶发烫,可适当降温 ④加热三颈烧瓶
(5)少量硫酰氯也可用氯磺酸(ClSO3H)分解获得,该反应的化学方程式为________________________,此方法得到的产品中会混有硫酸。从分解产物中分离出硫酰氯的方法是___________________。
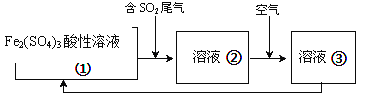
(6)工业上处理SO2废气的方法很多,例如可以用Fe2(SO4)3酸性溶液处理,其工艺流程如下溶液②转化为溶液③发生反应的离子方程式为__________________________ ;
有的工厂用电解法处理含有SO2的尾气,其装置如下图所示(电极材料均为惰性电极)。下列说法不正确的是_______
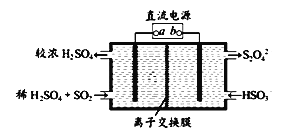
A.电极a连接的是电源的正极
B.若电路中转移0.03mole-,则离子交换膜左侧溶液中增加0.03mol离子
C.图中的离子交换膜是阳离子交换膜
D.阴极的电极反应式为2HSO3-+2e-+2H+==S2O42-+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E五种元素的原子序数依次增大,A原子无中子,B的单质在空气中含量最多,C、D元素同主族且原子序数D为C的二倍,E元素的价电子排布式为(n﹣l)d10+6ns1 , 回答下列问题:
(1)元素B在周期表中的位置是 .
(2)D元素基态原子的外围电子排布式为 .
(3)BC ![]() 的立体构型为 .
的立体构型为 .
(4)A元素与C元素形成两种常见的化合物,其原子个数比分别为2:1和1:1,两种化合物可以任意比互溶,原因是;其中一种化合物可在酸性条件下将KMnO4还原为Mn2+ , 写出相关反应的离子方程式:
(5)将过量BA3气体通入含E2+溶液中充分反应后生成的二价阳离子是(填离子符号),Imol该离子中含σ键为mol.
查看答案和解析>>
科目:高中化学 来源: 题型:
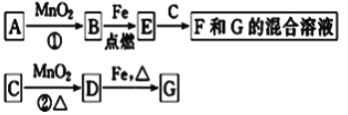
【题目】A~G各物质间的关系如图,其中B为可使带火星木条复燃的气态单质、D为黄绿色气态单质。
请回答下列问题:
(1)物质B和D分别为__________________________
(2)MnO2在反应①和②中的作用分别是______________________________
(3)新配制的F溶液应加入_____以防止其转化为G.检验G溶液中阳离子的常用试剂是________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A是一元羧酸,由C,H,O元素组成,质量分数:C%40%;H 6.67%;取0.60g A配成溶液,用含0.01mol NaOH 的溶液能恰好完全中和.
(1)A的最简式为;最简式量为 .
(2)A的相对分子质量为;分子式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在催化剂作用下,用乙醇制乙烯,乙醇转化率和乙烯选择性(生成乙烯的物质的量与乙醇转化的物质的量的比值)随温度、乙烯进料量(单位: ![]() )的关系如图所示(保持其他条件相同)。
)的关系如图所示(保持其他条件相同)。
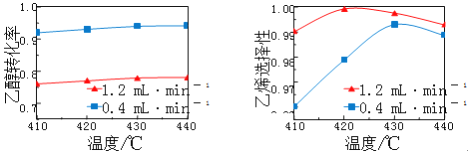
在410~440℃温度范围内,下列说法不正确的是
A. 当乙醇进料量一定,随乙醇转化率增大,乙烯选择性升高
B. 当乙醇进料量一定,随温度的升高,乙烯选择性不一定增大
C. 当温度一定,随乙醇进料量增大,乙醇转化率减小
D. 当温度一定,随乙醇进料量增大,乙烯选择性增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同温度下,体积均为1L的两个恒容密闭容器中发生可逆反应:N2(g)+3H2(g)![]() 2NH3(g) △H=-92.6kJ/mol.测得数据如表
2NH3(g) △H=-92.6kJ/mol.测得数据如表
容器编号 | 起始时各物质物质的量/mol | 达到平衡时体系能量的变化 | ||
N2 | H2 | NH3 | ||
(1) | 2 | 3 | 0 | 27.78kJ |
(2) | 1.6 | 1.8 | 0.8 | Q |
下列叙述不正确的是
A.容器(1)(2)反应达平衡时压强相等
B.容器(2)中反应开始时v(正)>v(逆)
C.容器(2)中反应达平衡时,吸收的热量Q为9.26kJ
D.若条件为“绝热恒容”,容器(1)中反应达平衡时n(NH3)<0.6mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用括号中注明的方法分离下列各组混合物,其中不正确的是( )
A. 汽油和煤油(蒸馏) B. 食盐中的沙子(溶解过滤)
C. 氯化钠和水(过滤) D. 花生油和水(分液)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com