
 N2O4达平衡时,测得混合气体的密度是相同条件下氢气的36倍,求:
N2O4达平衡时,测得混合气体的密度是相同条件下氢气的36倍,求: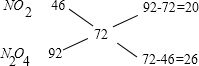
 2NO2
2NO2 | 5mol |
| 18mol |


科目:高中化学 来源:三点一测丛书 高中化学(选修)化学反应原理 江苏版课标本 江苏版课标本 题型:021
|
在某温度下,将2 mol A和3 mol B充入一密闭容器中,发生如下可逆反应:aA(g)+B(g) | |
A. |
60% |
B. |
24% |
C. |
4% |
D. |
40% |
查看答案和解析>>
科目:高中化学 来源:读想用 高二化学(上) 题型:038
某温度下,可逆反应2NO2![]() N2O4达平衡时,测得混合气体的密度是相同条件下氢气的36倍.求:
N2O4达平衡时,测得混合气体的密度是相同条件下氢气的36倍.求:
(1)此混合气体中NO2和N2O4的物质的量之比.
(2)混合气体中NO2的体积百分含量.
(3)混合气体中NO2和N2O4的质量之比.
(4)若反应的温度与体积不变,开始时输入的气体是N2O4,则平衡时的压强是起始时压强的多少倍?
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:2009-2010学年河北省唐山一中高二(上)开学调研化学试卷(9月份)(解析版) 题型:解答题
 N2O4达平衡时,测得混合气体的密度是相同条件下氢气的36倍,求:
N2O4达平衡时,测得混合气体的密度是相同条件下氢气的36倍,求:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com