
【题目】下列描述中,不符合生产实际的是( )
A.电解熔融的氧化铝制取金属铝,用铁做阳极
B.电解法精炼粗铜,用纯铜做阴极
C.电解饱和食盐水制烧碱,用涂镍碳钢网做阴极
D.在镀件上电镀锌,用锌做阳极
科目:高中化学 来源: 题型:
【题目】列式计算:标准状况下,22.4LHCl气体溶于50mL水再配成250mL溶液,
(1)求溶质的物质的量?
(2)求所得盐酸的物质的量浓度?
(3)若将此溶液再稀释成1L溶液,求稀释后盐酸的物质的量浓度?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产和生活密切相关,下列说法正确的是( )
A.乙烯是化学物质,不可用作水果的催熟剂
B.煤经过气化和液化等物理变化可转化为清洁燃料
C.石油是混合物,经分馏后得到汽油、煤油和柴油等纯净物
D.汽油与水互不相溶,但不可以用裂化汽油萃取溴水中的溴
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个密闭容器中,盛有N2和H2 , 它们的起始浓度分别是1.8molL﹣1和5.4molL﹣1 , 在一定的条件下它们反应生成NH3 , 10min后测得N2的浓度是0.8molL﹣1 , 则在这10min内NH3的平均反应速率是( )
A.0.1molL﹣1min﹣1
B.0.3molL﹣1min﹣1
C.0.2molL﹣1min﹣1
D.0.6molL﹣1min﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭体积不变的真空容器中加入一定量纯净的氨基甲酸铵固体,(固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)2NH3(g)+CO2(g),已知25℃时,平衡气体总浓度为2.4×10﹣3molL﹣1 , 下列说法中正确的是( )
A.密闭容器中气体的平均相对分子质量不变则该反应达到平衡状态
B.20℃时,氨基甲酸铵的分解平衡常数为2.048×10﹣9mol3L﹣3
C.恒温下压缩体积,NH3的体积分数不变
D.再加入一定量氨基甲酸铵,可加快正反应反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂实验室用CO和H2制备CH3OH,其原理为:CO(g)+2H2(g)CH3OH(g)△H<0该温度下的化学平衡常数表达式;若在298K、398K时化学平衡常数分别为K1、K2 , 则K1K2(填“>”、“<”、“=”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是电解CuCl2溶液的装置,其中c、d为石墨电极,则下列有关判断正确的是( ) 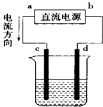
A.a为负极,b为正极
B.d为阳极,c为阴极
C.电解过程中,d电极质量增加
D.电解过程中,氯离子浓度不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.水和双氧水是相同的元素组成的物质,所以是同素异形体
B.氕、氘、氚互为同位素,其性质都相同
C.甲苯和邻二甲苯不是同系物
D.C5H12 存在一种同分异构体其一氯代物只有一种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com