
(6分)某同学购买了一瓶××牌“84消毒液”,查阅相关资料 和消毒液包装说明得到如下信息:“84消毒液”:含25%NaClO 1 000 mL、密度1.19 g·cm-3。
请根据以上信息和相关知识回答下列问题:
(1)该“84消毒液”的物质的量浓度为 mol·L-1(保留两位有效数字)。
(2)某实验需用480 mL含25%NaClO的消毒液。该同学参阅该“84消毒液”的配方,欲用NaClO固体配制该消毒液。
①下列说法正确的是 。
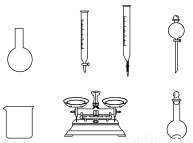
A.如上图所示的仪器中,有四种是不需要的,还需一种玻璃仪器
B.容量瓶用蒸馏水洗净后,应烘干才能用于溶液配制
C.利用久置的NaClO来配制可能导致结果偏低
D.需要称量的NaClO固体质量为143 g
②在配制过程中,下列操作可能使配制的溶液的浓度偏大的是 。
A.烧杯中溶液转移到容量瓶中时,未洗涤烧杯
B.定容时,俯视刻度线
C.定容时,仰视刻度线
D.移液时,有少量液体溅出
(1)4.0 (2) ①C ②B(每空2分)
【解析】
试题分析:(1)根据c=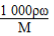 ,所以c(NaClO)=
,所以c(NaClO)=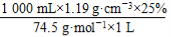 =4.0 mol·L-1;
=4.0 mol·L-1;
(2)①A、配制溶液,不需要分液漏斗、滴定管、烧瓶,但还需要玻璃棒和胶头滴管两种玻璃仪器,错误;B、容量瓶内有少量的蒸馏水对实验结果无影响,因为配制过程中需要加入水,不必烘干,错误;C、久置的次氯酸钠在空气中与二氧化碳、水反应而变质,所以次氯酸钠的质量减少,所配溶液的浓度偏低,正确;D、用480 mL含25%NaClO的消毒液,需配制500mL的溶液,所以次氯酸钠的质量是0.5L×4mol/L×74.5g/mol=149g,错误,所以答案选C;
②由c= 判断:A、D选项中使n偏小,浓度偏小;B选项中俯视刻度线,使V偏小,浓度偏大;C选项中仰视刻度线,使V偏大,浓度偏小,所以答案选B。
判断:A、D选项中使n偏小,浓度偏小;B选项中俯视刻度线,使V偏小,浓度偏大;C选项中仰视刻度线,使V偏大,浓度偏小,所以答案选B。
考点:考查物质的量浓度与质量分数的关系,溶液的配制、计算、误差分析


 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案科目:高中化学 来源:2014-2015福建省高一上学期期中化学试卷(解析版) 题型:选择题
设NA代表阿伏加德罗常数,下列说法正确的是
A.含0.2NA个氮原子的氮气物质的量为0.1mol
B.标准状况下,18g水所具有的体积为22.4L
C.11.2L氦气所含的分子数目为0.5NA
D.1mol的NaCl溶解在1L的水中可以得到1mol/L的NaCl溶液
查看答案和解析>>
科目:高中化学 来源:2014-2015浙江省高一上学期期中考试化学试卷(解析版) 题型:选择题
已知:还原性强弱:I- >Fe2+,往100 mLFeI2溶液中缓慢通入3.36 L(标准状况)氯气,反应完成后溶液中有1/2的Fe2+ 被氧化成Fe3+,则原FeI2溶液的物质的量浓度为
A.1.1mol·L-1 B.1.5mol·L-1 C.1.2mol·L-1 D.1.0mol·L-1
查看答案和解析>>
科目:高中化学 来源:2014-2015浙江省高一上学期期中考试化学试卷(解析版) 题型:选择题
某元素R的阴离子R2-核外共有a个电子,核内有b个中子,则能正确表示R原子符号的是
A. R B.
R B. R C.
R C. R D.
R D. R
R
查看答案和解析>>
科目:高中化学 来源:2014-2015浙江省高一上学期期中考试化学试卷(解析版) 题型:选择题
下列关于科学家及其提出学说与贡献的叙述不对应的是
A.道尔顿提出原子学说
B.汤姆生发现电子,并提出原子结构轨道模型
C.舍勒发现了氯气
D.卢瑟福根据α粒子散射现象,提出了带核的原子结构模型
查看答案和解析>>
科目:高中化学 来源:2014-2015浙江省宁波市高一上学期期中化学试卷(解析版) 题型:选择题
某溶液中只含有Na+、Al3+、Cl-、SO42- 四种离子,已知前三种离子的个数比为3∶2∶1,则溶液中Al3+和 SO42-的离子个数比为
A.1∶2 B.1∶4 C.3∶4 D.3∶2
查看答案和解析>>
科目:高中化学 来源:2014-2015浙江省宁波市高一上学期期中化学试卷(解析版) 题型:选择题
下列物质与其用途相符合的是
①Cl2——做消毒剂 ②AgBr——制胶卷,感光纸 ③AgI——人工降雨
④加碘食盐——预防甲状腺肿大 ⑤淀粉——检验I2的存在 ⑥NaClO——漂白纺织物
A.②③④⑤⑥ B.①②③④⑤ C.②③④⑤ D.全部
查看答案和解析>>
科目:高中化学 来源:2014-2015浙江省临海市高一上第一次段考化学试卷(解析版) 题型:计算题
现有含0.3mol氯化钡的氯化钡溶液和足量硝酸银溶液完全反应,求:
(1)写出反应的化学方程式(1分);
(2)求生成沉淀的质量(2分);
查看答案和解析>>
科目:高中化学 来源:2014-2015河北省高二上学期期中化学(理)试卷(解析版) 题型:选择题
碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。锌—锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为: Zn(s)+2MnO2(s)+H2O(l)==Zn(OH)2(s)+Mn2O3(s)下列说法错误的是
A.电池工作时,锌失去电子
B.电池正极的电极反应式为:2MnO2(s)+H2O(1)+2e—=Mn2O3(s)+2OH—(aq)
C.电池工作时,电子由正极通过外电路流向负极
D.外电路中每通过O.2mol电子,锌的质量理论上减小6.5g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com