
| A. | Fe2(SO4)3═2Fe3++3SO42- | B. | NaHCO3═Na++H++CO32- | ||
| C. | Ca(OH)2═Ca2++2OH- | D. | NaHSO4═Na++H++SO42- |
分析 先判断强弱电解质,强电解质完全电离,电离方程式用等号,弱电解质部分电离,电离方程式用可逆号,据此进行解答.
解答 解:A.Fe2(SO4)3为强电解质,在溶液中完全电离,其电离方程式为:Fe2(SO4)3═2Fe3++3SO42-,故A 正确;
B.NaHCO3在溶液中完全电离,其电离方程式为:NaHCO3═Na++HCO3-,故B错误;
C.Ca(OH)2在溶液中完全电离出钙离子和氢氧根离子,其电离方程式为:Ca(OH)2═Ca2++2OH-;故C正确;
D.NaHSO4为强电解质,在溶液中完全电离,其电离方程式为:NaHSO4═Na++H++SO42-;故D正确;
故选B.
点评 本题考查了电离方程式的书写,题目难度不大,正确判断强弱电解质为解答关键,注意掌握电离方程式的书写原则,试题有利于培养学生的规范答题能力.


科目:高中化学 来源: 题型:选择题
| A. | 2mol/L | B. | 1 mol/L | C. | 0.01 mol/L | D. | 0.22 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 58.5g NaCl溶于1L水中配得1mol/L NaCl溶液 | |
| B. | 在标准状况下,44.8LHCl气体溶于水配成1L溶液,所得溶液中溶质的物质的量浓度为2mol/L | |
| C. | 在标准状况下,22.4L氨气溶于水配成1L溶液,从所得溶液中取出10mL,其物质的量浓度为1mol/L | |
| D. | 1mol/L的CaCl2溶液1L,取出100mL,含0.2molCl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ⑥⑤③②① | B. | ⑦⑤③①② | C. | ④⑤③②①⑨ | D. | ⑥⑤①③② |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
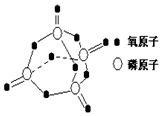 研究表明,化学反应的能量变化(△H)与反应物和生成物的键能有关.键能可以简单的理解为断开1 mol 化学键时所需吸收的能量.表是部分化学键的键能数据:
研究表明,化学反应的能量变化(△H)与反应物和生成物的键能有关.键能可以简单的理解为断开1 mol 化学键时所需吸收的能量.表是部分化学键的键能数据:| 化学键 | P-P | P-O | O=O | P=O |
| 键能/kJ•mol-1 | 197 | 360 | 499 | X |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属钠与O2反应,条件不同,产物不同 | |
| B. | 少量钠可保存在煤油中 | |
| C. | 金属钠质软,可以用小刀切割 | |
| D. | 由于钠很活泼,所以它能从水溶液中置换出金属活动性顺序表中排在钠后面的金属 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 如图为某化学反应的速率与时间的关系示意图.在t1时刻升高温度或者增大压强,速率的变化都符合的示意图的反应是( )
如图为某化学反应的速率与时间的关系示意图.在t1时刻升高温度或者增大压强,速率的变化都符合的示意图的反应是( )| A. | 2SO2(g)+O2(g)?2SO3(g) H<0 | B. | 4NH3(g)+5O2(g)?4NO(g)+6H2O(g) H<0 m | ||
| C. | H2(g)+I2(g)?2HI(g) H>0 | D. | N2(g)+3H2(g)?2 NH3(g) H<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com