
下列说法不正确的是
A.乙烯、乙醇均能使酸性高锰酸钾溶液褪色
B.通过乙烷的取代反应或乙烯的加成反应都可以制取纯净的氯乙烷
C.淀粉、纤维素都属于糖类,它们通式相同,但它们不互为同分异构体
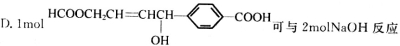
科目:高中化学 来源:2014-2015河北省唐山市高二下学期开学调研化学试卷(解析版) 题型:选择题
某学生的实验报告所列出的下列数据中合理的是
A.用10mL量筒量取7.13mL稀盐酸
B.用托盘天平称量25.20g NaCl
C.用广泛pH试纸测得某溶液的pH为2.3
D.用25mL滴定管做中和滴定时,用去某浓度的碱溶液21.70mL
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省广安市高三二诊理综化学试卷(解析版) 题型:实验题
(13分)二氧化氯(ClO2)是目前国际上公认的第四代高效、无毒的消毒剂,是一种黄绿色的气体,其熔点为-59 ℃,沸点为11.0 ℃,易溶于水。工业上用稍潮湿的KClO3和草酸(H2C2O4)在60 ℃时反应制得。某学生拟用下图所示装置模拟工业制取并收集ClO2。
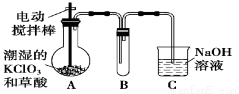
(1)A装置必须添加温度控制装置,除酒精灯外,还需要的玻璃仪器有烧杯、__________。
(2)B装置必须放在冰水浴中,其原因是______________________________。
(3)反应后在装置C中可得NaClO2溶液。已知:NaClO2饱和溶液在温度低于38℃时析出晶体是NaClO23H2O,高于38℃时析出晶体是NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。NaClO2的溶解度曲线如图
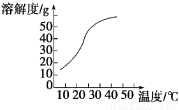
获得NaClO2晶体的操作步骤为:
①减压,55℃蒸发结晶;
②趁热过滤;
③ ;
④在55℃干燥,得到成品。
(4)ClO2很不稳定,需随用随制,产物用水吸收得到ClO2溶液。为测定所得溶液中ClO2的浓度,进行了下列实验:
步骤1:准确量取ClO2溶液10.00 mL,稀释成100.00 mL试样,量取V1 mL试样加入到锥形瓶中;
步骤2:用稀硫酸调节试样的pH≤2.0,加入足量的KI晶体,静置片刻;
步骤3:加入指示剂,用c mol·L-1 Na2S2O3溶液滴定至终点。重复2次,测得消耗Na2S2O3溶液平均值为V2 mL(已知2Na2S2O3+I2===Na2S4O6+2NaI)。
①配制100 mL c mol·L-1 Na2S2O3标准溶液时,用到的玻璃仪器除烧杯、量筒、玻璃棒外还有:_______。
②若步骤2所得溶液放置时间太长,则测定结果____________(填“偏高”、“偏低”或“不变”)
③ClO2溶液的浓度为________ g·L-1(用含字母的代数式表示)。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省德阳市高三“二诊”考试化学试卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数的值。下列叙述正确的是
A.1mol C(金刚石)中含有C—C键的数目为4NA
B.标准状况下,22.4L乙烯中含有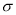 键的数目为5NA
键的数目为5NA
C.含0.2molH2SO4的浓硫酸与足量铜充分反应,生成SO2分子的数目为0.1NA
D.电解精炼铜时,若阳极质量减少32g,则阴极得到电子的数目为NA
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省济宁市高三第一次模拟考试理综化学试卷(解析版) 题型:填空题
(18分)氮、硫、氯及其化合物是中学化学重要的组成部分。
(1)氨气燃料电池使用的电解质溶液是KOH溶液,电池反应为: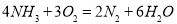 。该电池负极的电极反应式为__________;用该电池进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,以CuSO4溶液为电解质溶液,下列说法正确的是____________.
。该电池负极的电极反应式为__________;用该电池进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,以CuSO4溶液为电解质溶液,下列说法正确的是____________.
a.电能全部转化为化学能
b.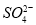 的物质的量浓度不变(不考虑溶液体积变化)
的物质的量浓度不变(不考虑溶液体积变化)
c.溶液中Cu2+向阳极移动
d.利用阳极泥可回收Ag、Pt、Au等金属
e.若阳极质量减少64g,则转移电子数为2NA个
(2)①将SO2通入到BaCl2溶液中,出现了异常现象,看到了明显的白色沉淀,为探究该白色沉淀的成分,他设计了如下实验流程:所得悬浊液 白色沉淀
白色沉淀 观察现象并判断。则试剂A的化学式为_________。实验表明,加入试剂A后,白色沉淀未见溶解,产生该白色沉淀的离子方程式是___________。
观察现象并判断。则试剂A的化学式为_________。实验表明,加入试剂A后,白色沉淀未见溶解,产生该白色沉淀的离子方程式是___________。
②利用如图所示电化学装置吸收工业尾气中SO2,阴极上生成Cu。写出装置中阳极的电极反应式__________。

(3)已知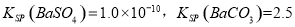
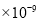 。某同学设想用下列流程得到BaCl2,
。某同学设想用下列流程得到BaCl2,
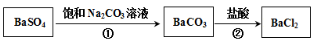
则①的离子方程式为_________,该反应的平衡常数K=__________;
(4)自来水厂用ClO2处理后的水中,要求ClO2的浓度在0.1~0.8mg·L-1之间。碘量法可以检测水中ClO2的浓度,步骤如下:
I.取一定体积的水样,加入一定量的碘化钾,再用氢氧化钠溶液调至中性,并加入淀粉溶液,溶液变蓝。
Ⅱ.加入一定量的Na2S2O3溶液,发生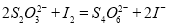 反应
反应
Ⅲ.加硫酸调节水样pH至1~3。
操作时,不同pH环境中粒子种类如图所示:
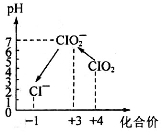
请回答:
①确定操作Ⅱ完全反应的现象是___________。
②在操作Ⅲ过程中,溶液又呈蓝色,反应的离子方程式是__________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省济南市高三下学期一模考试理综化学试卷(解析版) 题型:填空题
(12分)【化学——物质结构与性质】硼在半导体工业中被大量用作半导体掺杂物,同时含硼化合物在杀虫剂、防腐剂及新型储氢材料的制造中也有重要的地位。请回答下列问题:
(1)在第2周期的元素中,基态原子的第一电离能小于硼的元素有_________种。
(2)硼砂是人们最早使用的含硼化合物之一,其阴离子Xm-( Xm-中只含B、O、H三种元素)的球棍模型如图所示,则在Xm-中,硼原子轨道的杂化类型分别为_____、_____;图中标注为2号的原子与相邻原子成键形成的键角_____4号原子与相邻原子成键形成的键角(填“大于”“小于”或“等于”)。在下列各项中,在Xm-内不存在的化学键是____(填下列序号字母)。
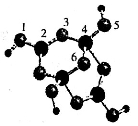
a.离子键 b.共价键 c.配位键
(3)氨硼烷(NH3BH3)与镧镍合金(LaNix)都是优良的储氢材料。镧镍合金的晶胞结构示意图如图所示(只有1个原子位于晶胞内部),则x=____。氨硼烷在高温下释放氢后生成的立方氮化硼晶体,具有类似金刚石的结构,硬度略小于金刚石。则在下列各项中,立方氮化硼晶体不可用作______(填下列序号字母)。
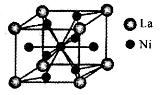
a.耐磨材料 b.切削工具 c.导电材料 d.钻探钻头
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省济南市高三下学期一模考试理综化学试卷(解析版) 题型:选择题
下列关于反应4Li+2SOC12===4LiCl+S+SO2的叙述中,不正确的是
A.SOCl2是氧化剂,Li是还原剂
B.2 mol SOCl2参加反应,共转移4 mol电子
C.将该反应设计成电池,SOCl2在正极发生反应
D.若将该反应设计成电池,可用稀硫酸作电解质溶液
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东肥城市高三一模理综化学试卷(解析版) 题型:推断题
(12分)【化学一有机化学基础】有机物F的合成路线如图所示:

已知以下信息:
(1)RCOOR’ RCH2OH (2)
RCH2OH (2)
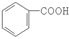
回答以下问题:
(1)A的结构简式为_____________________,G的结构简式为_____________________。
(2)B生成C的化学方程式为_____________________。
(3)检验E中含氧官能团的试剂是___________________,现象是___________________。
(4)E→F的反应类型是_____________________。
(5)写出A的一种符合下列条件的同分异构体的结构简式_____________________。
①属于芳香族化合物
②苯环上有四个取代基
③苯环上的一溴取代物只有一种
查看答案和解析>>
科目:高中化学 来源:2014-2015浙江省湖州市高三上学期期末考试化学试卷(解析版) 题型:选择题
下列说法正确的是
A.溴水能与聚乙烯反应褪色
B.谷氨酸的结构简式为: 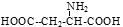
C.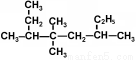 的系统名称为:3,4,4-三甲基-6-乙基庚烷
的系统名称为:3,4,4-三甲基-6-乙基庚烷
D.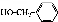 与
与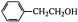 互为同系物
互为同系物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com