
����Ŀ������֪t��ʱAgCI��Ksp��2��10��10������t��ʱAg2CrO4��ˮ�еij����ܽ�ƽ��������ͼ��ʾ������˵����ȷ����

A����t��ʱ��Ag2CrO4��KspΪ1��10��9
B���ڱ���Ag2CrO4��Һ�м���K2CrO4��ʹ��Һ��Y�㵽X��
C����t��ʱ����0.01 mol/LAgNO3��Һ�ζ�20 mL 0.01 mol/L KCI��0.01 mol/L��K2CrO4�Ļ����Һ��CrO42���ȳ���
D����t��ʱ����ӦAg2CrO4(s)��2Cl��(aq)![]() 2AgCl(s)��CrO42��(aq)��ƽ�ⳣ��K��2.5��107
2AgCl(s)��CrO42��(aq)��ƽ�ⳣ��K��2.5��107
���𰸡�D
��������
���������A������ͼ�������ϵ����ݽ���ܶȻ������������õ��������ϵĵ��dz����ܽ�ƽ�⣬Ag2CrO4�ij����ܼ�ƽ��Ϊ��Ag2CrO4��s��![]() 2Ag+CrO42-��Ksp��c2��Ag+��c��CrO42-������10-3��2��10-6��10-12����A����B���ڱ���Ag2CrO4��Һ�м���K2CrO4��Ϊ������Һ�������������ϣ������ڱ���Ag2CrO4��Һ�м���K2CrO4����ʹ��Һ��Y���ΪX�㣬��B����C�������ܶȻ���������Ksp��CrO42-��=c2��Ag+��c��CrO42-��=1��10-12��Ksp��AgCl��=c��Ag+��c��Cl-��=1.8��10-10����0.01mol/L AgNO3��Һ�ζ�20mL0.01mol/L KCl��0.01mol/L��K2CrO4�Ļ����Һ��c��CrO42-��=0.01mol/L���õ�c��Ag+����10��12��0.01��10-5mol/L��0.01mol/L KCl��Һ�У�c��Cl-����0.01mol/L�������ܶȻ�����õ���c��Ag+����2��1010��0.01��2��10-8mol/L�������������Ȼ�����������C������D����t��ʱ����ӦAg2CrO4(s)��2Cl��(aq)
2Ag+CrO42-��Ksp��c2��Ag+��c��CrO42-������10-3��2��10-6��10-12����A����B���ڱ���Ag2CrO4��Һ�м���K2CrO4��Ϊ������Һ�������������ϣ������ڱ���Ag2CrO4��Һ�м���K2CrO4����ʹ��Һ��Y���ΪX�㣬��B����C�������ܶȻ���������Ksp��CrO42-��=c2��Ag+��c��CrO42-��=1��10-12��Ksp��AgCl��=c��Ag+��c��Cl-��=1.8��10-10����0.01mol/L AgNO3��Һ�ζ�20mL0.01mol/L KCl��0.01mol/L��K2CrO4�Ļ����Һ��c��CrO42-��=0.01mol/L���õ�c��Ag+����10��12��0.01��10-5mol/L��0.01mol/L KCl��Һ�У�c��Cl-����0.01mol/L�������ܶȻ�����õ���c��Ag+����2��1010��0.01��2��10-8mol/L�������������Ȼ�����������C������D����t��ʱ����ӦAg2CrO4(s)��2Cl��(aq)![]() 2AgCl(s)��CrO42��(aq)��ƽ�ⳣ��
2AgCl(s)��CrO42��(aq)��ƽ�ⳣ��![]() ��2.5��107����D��ȷ����ѡD��
��2.5��107����D��ȷ����ѡD��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ���б���Ҫ�õ��¶ȼƵ��� �� ��
A. ��ʵ����������ʯ�� B. �ɱ����屽
C. �ɼױ���TNT D. �ɱ���һ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Co3O4���Ʊ�ʯīϩ�����������LiCoO2��ԭ�ϡ����ܿ�ʯ����Ҫ�ɷ�ΪCo3S4����������FeO��Fe2O3��Al2O3�����ʣ�Ϊԭ����ȡCo3O4�Ĺ����������£�
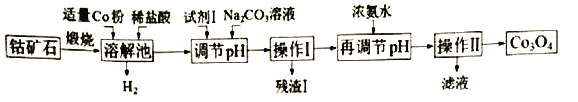
��֪��Co��FeΪ���ý�������������ǿ������˳��Ϊ��Co3+>Fe3+>Co2+��
��������������ܶȻ����±���
![]()
(l)д���ܽ��������H2�����ӷ�Ӧ����ʽ��____��
(2)�����Լ�1��Ŀ���ǽ�Fe2+����ΪFe3+���Լ�l��ѡ��__ ��
A���Ȼ��� B��˫��ˮ C���������� D.��ˮ
(3)����l����Ҫ�ɷ�Ϊ____����Ũ��ˮ�ٵ���pH��pHӦ�Դ���___ ������֪��lg2=0.3��������Ũ��С��l.0��l0-5mol/L������Ϊ������ȫ����
(4)���������____��____����������ĸ����裻�����з�Ӧ�Ļ�ѧ����ʽ _________��
(5)Ҫ�õ�15.0g��������Ϊ98%��LiCoO2�������ϣ���������ҪCo3O4������Ϊ __________g��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)���������ĸ���������ԭ�������ɴ�С��˳��������________��
��0.5 mol����
�ڱ�״����22.4 L����
��4 ��ʱ9 mLˮ
��0.2 mol������(Na3PO4)
(2)����m gij���壬������ԭ�ӷ��ӣ���Ħ������ΪM g��mol��1���������ӵ�������NA��ʾ���������Ϸ��ż���Ӧ������д���пո�
�ٸ���������ʵ���Ϊ________mol��
�ڸ���������ԭ������Ϊ________����
�۸������ڱ�״���µ����Ϊ________L��
�ܸ�������ȫ����ˮ�γ�V L��Һ(�����Ƿ�Ӧ)��������Һ�����ʵ���Ũ��Ϊ________mol��L��1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������ơ���װ��ʹ�÷�������ѧ��ѧʵ��Ļ�������ͼΪ����ʵ��װ�á�
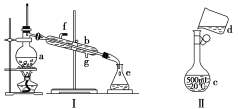
(1)д���������������ƣ�
a��________��b.________��c.________��
(2)����a��e�У�ʹ��ǰ�������Ƿ�©ˮ����________(�����)��
(3)������װ�â�������Ȼ�̼�;ƾ��Ļ����¶ȼ�ˮ�����λ����________��������ˮ��________(����f������g������ͬ)��ͨ�룬________��������
(4)��������0.125 mol��L��1 NaOH��Һ450 mL��װ�â���ijͬѧת����Һ��ʾ��ͼ��
��ͼ�еĴ�����__________________��
����ͼ�и�����������������ƽ�⣬Ϊ���ʵ�黹��Ҫ��������_________________________��
�ڸ��ݼ����֪�������NaOH������Ϊ__________________________g������ʱ���������ձ���������ҩƷ����ƽƽ�⣬��ֻȱ��������ʱ�������������_______________________________��
�����в���ʹ���Ƶ�NaOH��ҺŨ��ƫ�͵���________��
A����������������ϣ�NaOH���������Ͻ��г���(ʹ������)
B��ѡ�õ�����ƿ������������ˮ
C������ҡ�Ⱥ�Һ���½����ּ�ˮ���̶���
D���������ƹ����У�����ƿ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£��������pH��������Ȼ������Һ������˵����ȷ����
A. ����Һ����������ͬ
B. �ֱ��������ҵ�����п��Ӧ��ƽ����Ӧ���ʺ��ߴ�
C. �ֱ����Ũ�ȵ�����������Һ��Ӧ�����ԣ����ĵ��������Ƶ������ͬ
D. ϡ��10���������pH���Ȼ����Һ��pHС
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и��ֲ��������������ǽ������ϵ��ǣ� ��
A.�մ�
B.ˮ��
C.����
D.���ά
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1��������ijͬѧ�Ƶ���1molNa ����������ֵ�ϵ��� Na �����ԭ����������λȡ g���Ĺ� �������㲹�������������� m��Na ԭ������ʾһ�� Na ԭ�ӵ�������m��12C����ʾһ�� 12Cԭ�ӵ����� ��Ar ��ʾ Na �����ԭ��������NA ��ʾ�����ӵ�������
��Ϊ��m��Na ԭ����=1/12m��12C��Ar��������1molNa ԭ�ӵ�����=1/12________Ar=1/12_____ Ar=Ar g
��2���� CO2 �� CO ��ɵĻ������� H2 ������ܶ� 20������������ CO2 ���������Ϊ_____��CO ����������_______
��3����״������336L �� NH3 ���� 1L ˮ����������Һ���ܶ�Ϊ ag/cm3���������ʵ���Ũ��Ϊ����������ˮȫ��ת��Ϊ NH4CL������ 2mol/L ����������Ϊ_____��NH3��HCl=NH4Cl����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��̬��A���ܶ�����ͬ״���������ܶȵ�14�����л���A~E�ܷ�����ͼ��ʾһϵ�б仯��������˵���������
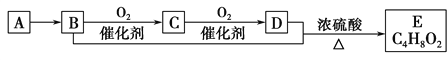
A. A����������ԭ�Ӿ���ͬһƽ����
B. C4H8O2��������ͬ���칹����4��
C. C��ˮ��Һ�ֳƸ������֣�����ɱ������������
D. �����ʵ�����B��D�������Ʒ�Ӧ��������������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com