
在加入铝粉能放出氢气的溶液中,下列各组离子可能大量共存的是
( )
A.NH NO
NO CO
CO Na+
Na+
B.Na+ Ba2+ Mg2+ HCO
C.NO K+ AlO
K+ AlO OH-
OH-
D.NO Mg2+ K+ Cl-
Mg2+ K+ Cl-
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源: 题型:
席夫碱类化合物G在催化、药物、新材料等方面有广泛应用。合成G的一种路线如下:

已知以下信息:
 | |||
 | |||
① 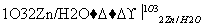 R1CHO+
R1CHO+
②1 mol B经上述反应可生成2 mol C,且C不能发生银镜反应
③D属于单取代芳烃,其相对分子质量为106
④核磁共振氢谱显示F苯环上有两种化学环境的氢
 |
⑤ +H2O
回答下列问题:
(1)由A生成B的化学方程式为__________________,反应类型为________________。
(2)D的化学名称是________,由D生成E的化学方程式为________________________________________________________________________。
(3)G的结构简式为______________________________________________。
(4)F的同分异构体中含有苯环的还有________种(不考虑立体结构),其中核磁共振氢谱为4组峰,且面积比为6∶2∶2∶1的是____________(写出其中一种的结构简式)。
(5)由苯及化合物C经如下步骤可合成N异丙基苯胺。
 |
N异丙基苯胺
反应条件1所选用的试剂为________________,反应条件2所选用的试剂为______________,Ⅰ的结构简式为_________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
高纯MnCO3是制备高性能磁性材料的主要原料。实验室以MnO2为原料制备少量高纯MnCO3的操作步骤如下:
查阅资料:①MnCO3难溶于水,潮湿时易被空气氧化,100℃开始分解。
②Mn(OH)2开始沉淀时pH=7.7。
实验过程:
Ⅰ. 用图1所示装置制备MnSO4溶液。
Ⅱ. 边搅拌边向MnSO4溶液中加入稍过量NaHCO3溶液,过滤。
Ⅲ. 洗涤沉淀。
Ⅳ. 洗涤后的沉淀在温度低于100℃的条件下干燥,制得高纯MnCO3固体。
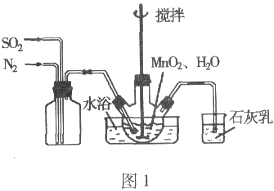
(1)图1中石灰乳的作用是__________,烧瓶中发生反应的化学方程式是__________。
(2)根据图2“浸锰”的反应适宜时间是____________________。若实验中将N2换成空气,测得反应液中Mn2+、SO42-的浓度随反应时间t变化如图3。导致溶液中Mn2+、SO42-浓度变化产生明显差异的原因是______________________________。

图2 图3
(3)Ⅱ中加入稍过量NaHCO3溶液,控制溶液pH在__________范围,写出加入NaHCO3,后发生反应的离子方程式____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
有关氨气的实验较多,下面对这些实验原理的分析中,正确的是( )
A、氨气极易溶于水,可以用来做喷泉实验
B、氨气的还原性可以解释氨气与氯化氢的反应实验
C、NH3·H2O不稳定,实验室可用NH4Cl和石灰水制取氨气
D、NH3液化时放出大量的热,因而,不能用氨作制冷剂
查看答案和解析>>
科目:高中化学 来源: 题型:
用含少量镁粉的铝粉制取纯净的氢氧化铝,下述操作步骤中最恰当的组合是( )
①加盐酸溶解;②加烧碱溶液溶解;③过滤;④通入过量CO2生成Al(OH)3沉淀;⑤加入盐酸生成Al(OH)3沉淀;⑥加入过量烧碱溶液
A.①⑥⑤③ B.②③④③
C.②③⑤③ D.①③⑤③
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关铝及其化合物的叙述正确的是( )
A.铝粉与三氧化钨共热可制取金属钨
B.足量铝分别与含1 mol HCl、1 mol NaOH的溶液反应,产生相同量的氢气
C.工业上用电解熔融Al2O3的方法冶炼铝
D.在浓硝酸中加入等体积的浓硫酸后,立即加入铝片,铝片表面发生钝化
查看答案和解析>>
科目:高中化学 来源: 题型:
化学与生活、社会密切相关。下列说法不正确的是( )
A.利用太阳能等清洁能源代替化石燃料,有利于节约资源、保护环境
B.凡含有食品添加剂的食物对人体健康均有害,不可食用
C.为防止电池中的重金属等污染土壤和水体,应积极开发废电池的综合利用技术
D.提倡人们购物时不用塑料袋,是为了防止白色污染
查看答案和解析>>
科目:高中化学 来源: 题型:
向恒温、恒容(2L)的密闭容器中充入2molX和一定量的Y,发生反应:2X(g)+Y(g) 2Z(g)
2Z(g)
ΔH<0,4min后达到平衡c(X)=0.2mol·L-1,且X与Y的转化率相等。下列说法中不正确的是( )
A.达到平衡时,再充入1molX,反应的焓变保持不变
B.用Y表示4min内的反应速率为0.1 mol·L-1·min-1
C.再向容器中充入1molZ,达到新平衡,c(X)∶c(Y)=2∶1
D.4min后,若升高温度,平衡常数K增大
查看答案和解析>>
科目:高中化学 来源: 题型:
草酸是二元弱酸,草酸氢钾溶液呈酸性。在0.1mol·L-1 KHC2O4溶液中,下列关系正确的是 ( )
A.c(K+)+c(H+) = c(HC2O4-)+c(OH-)+c(C2O42-)
B.c(HC2O4-)+c (C2O42-) = 0.1 mol·L-1
C.c(C2O42-) < c(H2C2O4)
D.c(K+) = c(H2C2O4)+c(HC2O4-)+c(C2O42-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com