
【题目】下列说法正确的是
A. 由C(石墨) = C(金刚石) △H=+1.9 kJ·mol-1可知,金刚石比石墨稳定
B. 在一定条件下,等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多
C. 已知2C(s) + O2(g) = 2CO(g) △H=-221 kJ·mol-1,可知C的标准燃烧热为110.5 kJ·mol-1
D. 在一密闭容器中,9.6 g的硫粉与11.2 g的铁粉混合加热,充分反应,生成硫化亚铁17.6 g,放出19.12 kJ的热量,则Fe(s) + S(s) = FeS(s) △H= - 95.6 kJ·mol-1
【答案】D
【解析】
A. 物质所具有的能量越低越稳定,因C(石墨) = C(金刚石) △H=+1.9 kJ·mol-1可知,石墨的能量比金刚石的低,则石墨比金刚石稳定,A项错误;
B. 在一定条件下,等物质的量的硫蒸气的能量比硫固体的能量高,则两者分别完全燃烧,前者放出的热量多,B项错误;
C. 燃烧热是在25°C,101 kPa时,1 mol可燃物完全燃烧生成稳定的化合物时所放出的热量,已知2C(s) + O2(g) = 2CO(g) △H=-221 kJ·mol-1,产物CO不是C的稳定氧化物,则不能求出标准燃烧热,C项正确;
D. 密闭容器中,9.6g硫粉物质的量=![]() =0.3mol,与11.2g铁粉物质的量=
=0.3mol,与11.2g铁粉物质的量=![]() = 0.2mol,混合加热生成硫化亚铁17.6g时,硫过量,放出19.12kJ 热量,所以1mol铁反应放热=19.12kJ ×
= 0.2mol,混合加热生成硫化亚铁17.6g时,硫过量,放出19.12kJ 热量,所以1mol铁反应放热=19.12kJ ×![]() =95.6kJ,热化学方程式为Fe(s)+S(s)═FeS(s)△H=-95.6kJ.mol-1,D项正确;
=95.6kJ,热化学方程式为Fe(s)+S(s)═FeS(s)△H=-95.6kJ.mol-1,D项正确;
答案选D。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】将Na2O2逐渐加入到含有H+、Mg2+、Al3+、NH4+的混合液中并微热,产生沉淀和气体的物质的量(mol)与加入的Na2O2物质的量(mol)的关系如图所示,则原溶液中的Mg2+、Al3+、NH4+物质的量分别为

A. 2 mol、3 mol、6 mol B. 3 mol、2 mol、6mol
C. 2 mol、3 mol、4 mol D. 3 mol、2 mol、2 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向X的溶液中,加入Y试剂,产生的沉淀示意图如图所示情形的是(注意线段的斜率)
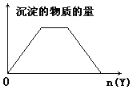
A. 向含NaOH的NaAlO2溶液中滴加盐酸
B. 向HCl和AlCl3的混合液中滴加NaOH
C. 向NH4Cl和AlCl3的混合液中滴加NaOH
D. 向NaOH和Ca(OH)2的混合液中通入CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】解释下列事实的方程式不正确的是
A. 纯碱溶液遇酚酞变红:CO32-+H2O![]() HCO3-+OH-
HCO3-+OH-
B. 以石墨为电极电解MgCl2溶液:2Cl-+2H2O ![]() Cl2↑+H2↑+20H-
Cl2↑+H2↑+20H-
C. 纯碱溶液处理锅炉中的水垢:CaSO4(s)+CO32-(aq)![]() CaCO3(s)+SO42-(aq)
CaCO3(s)+SO42-(aq)
D. 在Fe(NO3)2溶液中加稀硫酸有气体产生:3Fe2++4H++NO3-=3Fe3++NO↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组提取三处被污染的水源进行了如下分析,给出了如下实验信息:其中一处被污染的水源含有A、B两种物质,一处含有C、D两种物质,一处含有E物质,A、B、C、D、E为五种常见化合物,均由下表中的离子形成:
阳离子 | K+ Na+ Cu2+ Al3+ |
阴离子 | SO42- HCO3- NO3- OH- |
为了鉴别上述化合物,分别完成以下实验,其结果是
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解;
③进行焰色反应,只有B、C为紫色(透过蓝色钴玻璃);
④在各溶液中加入硝酸钡溶液,再加入过量稀硝酸,A中放出无色气体,C、D中产生白色沉淀;
⑤将B、D两溶液混合,未见沉淀或气体生成。
根据上述实验填空:
(1)写出B、D的化学式:B________,D________。
(2)写出D、E发生反应的离子方程式:___________________________。
(3)将含1 mol A的溶液与含1 mol E的溶液反应后蒸干,仅得到一种化合物,该化合物为__________。
(3)C常用作净水剂,用离子方程式表示其净水原理:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图甲为在铜棒上电镀银的装置,图乙是在图甲装置中央放置质量相等的两个银圈,用绳子系住(绳子为绝缘体),一段时间后,两装置中铜极质量均增重1.08g。下列说法不正确的是
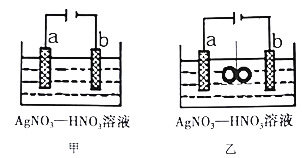
A. 电极a为纯银
B. 图甲:若b极有标况下112mL红棕色气体生成,则电子有效利用率为50%
C. 图乙:若乙池中无气体生成,则绳子两端银圈质量之差为2.16g
D. 处理银器表面的黑班(Ag2S),将银器置于盛有食盐水的铝制容器里并与铝接触,则Ag2S可以转化为Ag
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】当温度和压强一定时,决定气体体积大小的主要因素是( )
A. 分子数目的多少 B. 分子间距离的大小
C. 分子间引力的大小 D. 分子直径的大小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某100 mL混合酸溶液中,HNO3和H2SO4的物质的量浓度分别为0.2 mol·L-1和0.4 mol·L-1,向该混合溶液中加入2.24 g铁粉,加热充分反应后,下列说法不正确的是
A. 生成的气体在标准状况下的体积为672 mLB. 生成的气体有NO和H2
C. 所得溶液中有溶质FeSO4和Fe2(SO4)3D. 所得溶液中Fe2+的物质的量浓度为0.4 mol·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com