
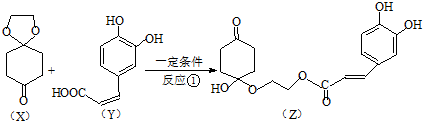
 )分子间脱水而得;一定条件下,M发生1个-OH的消去反应得到稳定化合物N(分子式为C6H8O2),则N的结构简式为
)分子间脱水而得;一定条件下,M发生1个-OH的消去反应得到稳定化合物N(分子式为C6H8O2),则N的结构简式为 (已知烯醇式不稳定,会发生分子重排,例如:
(已知烯醇式不稳定,会发生分子重排,例如: ).
).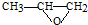 )发生类似反应①的反应,其生成物的结构简式为
)发生类似反应①的反应,其生成物的结构简式为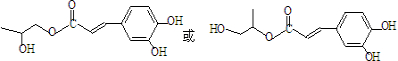 (写一种);
(写一种);分析 (1)由结构简式可知结构对称,含3种位置的H;
(2)A.X中不含苯环;
B.Y中苯环与碳碳双键与氢气发生加成反应;
C.Z中含碳碳双键、酚-OH、醇-OH;
D.Z中酚-OH、-COOC-与NaOH反应;
(3)Y中酚-OH的邻对位与溴水发生取代,碳碳双键与溴水发生加成;
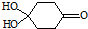
(4)X中含醚键,可由醇分子见脱水生成;一定条件下,M发生1个-OH的消去反应得到稳定化合物N,N中含碳碳双键与-OH相连,发生分子重排,生成环己二酮;
(5)反应①为取代反应,以此分析反应;Y的同分异构体很多种,其中有苯环、苯环上有四个取代基(官能团种类和数目不变且酚羟基的位置不变),则2个酚-OH相邻,苯环上还有两个取代基为-CH=CH2、-COOH,以此来解答.
解答 解:(1)由结构简式可知结构对称,含3种位置的H,则有3种化学环境不同的氢原子,故答案为:3;
(2)A.X中不含苯环,则不属于芳香化合物,故A错误;
B.Y中苯环与碳碳双键与氢气发生加成反应,则Ni催化下Y能与4mol H2加成,故B错误;
C.Z中含碳碳双键、酚-OH、醇-OH,则能发生加成、取代及消去反应,故C正确;
D.Z中酚-OH、-COOC-与NaOH反应,则1mol Z最多可与3mol NaOH反应,故D错误;
故答案为:C;
(3)Y中酚-OH的邻对位与溴水发生取代,碳碳双键与溴水发生加成,该反应为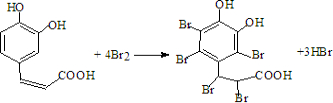 ,所以Y与过量的溴水反应后消耗的Br2的物质的量为4mol,
,所以Y与过量的溴水反应后消耗的Br2的物质的量为4mol,
故答案为:4mol;
(4)X中含醚键,可由醇分子见脱水生成,则X可由乙二醇与M合成;一定条件下,M发生1个-OH的消去反应得到稳定化合物N,N中含碳碳双键与-OH相连,发生分子重排,生成环己二酮,则N的结构简式为 ,故答案为:乙二醇;
,故答案为:乙二醇; ;
;
(5)反应①为取代反应,则Y与环氧丙烷(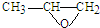 )发生类似反应①的反应后生成物的结构简式为
)发生类似反应①的反应后生成物的结构简式为 ;Y的同分异构体很多种,其中有苯环、苯环上有四个取代基(官能团种类和数目不变且酚羟基的位置不变),则2个酚-OH相邻,苯环上还有两个取代基为-CH=CH2、-COOH,由图
;Y的同分异构体很多种,其中有苯环、苯环上有四个取代基(官能团种类和数目不变且酚羟基的位置不变),则2个酚-OH相邻,苯环上还有两个取代基为-CH=CH2、-COOH,由图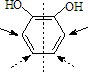 根据定一动一的原则可知,取代基-CH=CH2、-COOH在苯环上有6种位置,则同分异构体为6种,
根据定一动一的原则可知,取代基-CH=CH2、-COOH在苯环上有6种位置,则同分异构体为6种,
故答案为: ;6.
;6.
点评 本题考查有机物合成,为高频考点,把握官能团与性质的关系解答的关键,侧重羧酸、酯、烯烃和酚性质的考查,注意(5)中同分异构体推断为解答的难点,有利于学生综合应用知识的训练,题目难度中等.


 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素编号元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半径(10-10m) | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 1.43 |
| 最高或最低化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
| -2 | -3 | -1 | -3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向NaOH溶液中通入过量的SO2:SO2+20H-═SO32-+H20 | |
| B. | Na2O2和H2O反应:Na2O2+H2O═2Na++20H-+02↑ | |
| C. | Cl2和H2O反应:Cl2+H20═2H++Cl-+Cl0- | |
| D. | SiO2+2OH-═SiO32-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
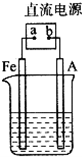 某地区常下酸雨,因而使金属制品锈蚀严重,铁制品镀铜可以有效防止铁的锈蚀,右图所示为铁制品镀铜的过程,请据此回答下列问题:
某地区常下酸雨,因而使金属制品锈蚀严重,铁制品镀铜可以有效防止铁的锈蚀,右图所示为铁制品镀铜的过程,请据此回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯和乙烷 | B. | 乙烷和丙烯 | C. | 甲烷和乙烯 | D. | 丙烯和丙烷 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com