
| A. | 当一个化学反应在一定条件下达到最大限度时,反应速率也最大 | |
| B. | 用一定量的锌片和足量的稀硫酸反应制氢气时,加入少量氧化铜,可以加快反应的速率且生成氢气的总量不变 | |
| C. | 燃烧一定是放热反应,也是氧化还原反应 | |
| D. | 化学反应中能量变化的大小与反应物的状态无关 |
分析 A.在一定条件下的可逆反应经过一段时间后,达到最大限度时,正、逆反应速率相等;
B.Zn与硫酸铜反应,与硫酸反应的锌会减少;
C.燃烧是可燃物与氧气反应;
D.等量的同种物质气态时能量最高,液态次之,固态能量最低.
解答 解:A.在一定条件下的可逆反应经过一段时间后,达到最大限度时,正、逆反应速率相等,但是反应速率不一定最大,反应速率与温度、浓度、催化剂等条件有关,故A错误;
B.Zn与硫酸铜反应,与硫酸反应的锌会减少,所以生成的氢气的体积会减少,故B错误;
C.燃烧是发光发热的剧烈的氧化还原反应,所以燃烧一定是放热反应,也是氧化还原反应,故C正确;
D.等量的同种物质气态时能量最高,液态次之,固态能量最低,所以化学反应中能量变化的大小与反应物的状态有关,故D错误.
故选C.
点评 本题考查了化学反应速率、金属与酸的反应、氧化还原反应、能量与物质状态的关系等,题目难度不大,侧重于基础知识的考查,注意基础知识的归纳整理.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 1:1 | B. | 2:1 | C. | 1:2 | D. | 无法计算 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2>N2>O2 | |
| B. | NH3>AsH3>PH3 | |
| C. | Cl2>Br2>I2 | |
| D. | C(CH3)4>(CH3)2CHCH2CH3>CH3CH2CH2CH2CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | R不是主族元素 | B. | R是第六周期元素 | ||
| C. | R的原子核内有63个质子 | D. | R的一种同位素的核内有89个中子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.4 g 金属镁变为镁离子时失去的电子数为0.1NA | |
| B. | 常温常压下,8.0g CH4中含有的价电子总数为5NA | |
| C. | 在标准状况下,22.4 L CH4与NH3混合气所含有的质子总数为10NA | |
| D. | 常温下,5.6g铁钉与足量浓硝酸反应,转移的电子数为0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ag2O作正极,被氧化 | |
| B. | 若将电解液换成酸性溶液,使用寿命会缩短 | |
| C. | Zn作正极,被还原 | |
| D. | OH-向正极移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2(CO):通O2,点燃 | B. | CO(CO2):通过NaOH溶液 | ||
| C. | N2(O2):通过灼热的CuO | D. | CaO(CaCO3):加水,再过滤 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
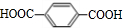 +2NaHCO3→
+2NaHCO3→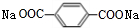 +2H2O+2CO2↑.
+2H2O+2CO2↑.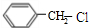 .
.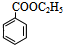 +H2O$→_{△}^{稀硫酸}$
+H2O$→_{△}^{稀硫酸}$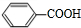 +CH3CH2OH.
+CH3CH2OH.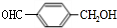 ,F与氢气1:1加成的芳香产物G中有3种氢,G与B发生聚合反应的化学方程式是n
,F与氢气1:1加成的芳香产物G中有3种氢,G与B发生聚合反应的化学方程式是n +n
+n $\stackrel{一定条件下}{→}$
$\stackrel{一定条件下}{→}$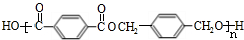 +(2n-1)H2O.
+(2n-1)H2O.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com