
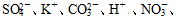 HCO3-��Cl���������е������֡�Ȼ�����������µ�ʵ�������
HCO3-��Cl���������е������֡�Ȼ�����������µ�ʵ������� ____________��
____________��
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��Na2CO3������ | B��FeCl3������ | C��CuSO4������ | D��Ca(NO3)2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���۲�K2SO4����ɫӦ����ɫ���ܲ��� |
| B��Na��NaCl������ʱ������ɫ��ͬ |
| C����������ɫ��Ӧ������NaCl��KCl |
| D����ɫ��Ӧһ��������ѧ�仯 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��AgI�ɱ����������˹����� |
| B�����������麬��ʳ�����Ƿ��е�Ԫ�� |
| C�����ᱵ���������͡�����ΪBa2+�� |
| D����ʯͷֽ������ǿ����ǿ��ĸ�ʴ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������ʱ��ij��Һ����ˮ���������c��H������c��OH�����ij˻�Ϊ1��10��24������Һ��һ�����Դ�������K����Na����AlO2����SO42�� |
| B��������Һ������ʵ���������������Һ��ϵ����ӷ���ʽΪ�� 3Ba2+ +6OH�� + 2Al3+ + 3SO42�� �T 3BaSO4��+ 2Al(OH)3�� |
| C����1L0.3mol/L��NaOH��Һ�л���ͨ��CO2��������Һ����8.8g������Һ�У� 3c��Na+��=2[c��HCO3����+c��CO32����+c��H2CO3��] |
| D��pH=5��������Һϡ�͵�ԭ����500����ϡ�ͺ�c��SO42������c��H+��֮��ԼΪ1��10 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��CO32�� | B��SO42�� | C��Mg2�� | D��Ba2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������ϡ���������ɫ��ζ���壬������ͨ�����ʯ��ˮ�У���Һ����ǣ���ԭ��Һ��һ����CO32�� |
| B����ij��Һ��ͨ��Cl2��Ȼ���ټ���KSCN��Һ���ɫ��˵��ԭ��Һ����Fe2�� |
| C����������������Һ�����ȣ�������ʹʪ��ĺ�ɫʯ����ֽ���������壬��ԭ��Һ��һ����NH4+ |
| D������ϡ�����ữ��AgNO3��Һ��������ɫ��������ԭ��Һ��һ������Cl�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 ����̼�������Һ�м���������NaOH��Һ��NH4+ +OH��= NH3��H2O
����̼�������Һ�м���������NaOH��Һ��NH4+ +OH��= NH3��H2O �鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com