
分析 设的N2 和H2的物质的量分别为xmol、ymol,则$\frac{28x+2y}{x+y}$=4.25×2,整理可得x:y=1:3,假设N2 和H2的物质的量分别为1mol、3mol,达到平衡时,NH3占25%,则:
N2(g)+3H2(g)?2NH3(g)
起始(mol):1 3 0
转化(mol):x 3x 2x
平衡(mol):1-x 3-3x 2x
所以$\frac{2x}{4-2x}$=25%,解得x=0.4
(1)相同条件下,气体体积之比等于其物质的量之比;
(2)转化率=$\frac{物质的量变化量}{起始物质的量}$×100%;
(3)混合气体总质量不变,容器容积不变,混合气体密度不变;
(4)恒温恒容下,压强之比等于气体物质的量之比.
解答 解:设的N2 和H2的物质的量分别为xmol、ymol,则$\frac{28x+2y}{x+y}$=4.25×2,整理可得x:y=1:3,假设N2 和H2的物质的量分别为1mol、3mol,达到平衡时,NH3占25%,则:
N2(g)+3H2(g)?2NH3(g)
起始(mol):1 3 0
转化(mol):x 3x 2x
平衡(mol):1-x 3-3x 2x
所以$\frac{2x}{4-2x}$=25%,解得x=0.4
(1)相同条件下,气体体积之比等于其物质的量之比,故进入容器N2和H2的 体积比为1mol:3mol=1:3,故答案为:1:3;
(2)氮气转化率=$\frac{0.4mol}{1mol}$×100%=40%,故答案为:40%;
(3)混合气体总质量不变,容器容积不变,混合气体密度不变,即反应前后的密度比为1:1,故答案为:1:1;
(4)恒温恒容下,压强之比等于气体物质的量之比,故反应前后的压强比为(1+3)mol:(4-0.8)mol=5:4,故答案为:5:4.
点评 本题考查化学平衡计算,关键是计算氮气与氢气起始物质的量之比,注意利用赋值法解答,注意三段式解题法在化学平衡计算中应用.


科目:高中化学 来源: 题型:解答题
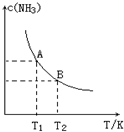 将1mol N2(g)和3mol H2(g)通入一个10L的恒容密闭容器中发生反应,在不同温度下达到平衡时NH3(g)的平衡浓度如图所示.其中温度为T1时平衡混合气体中氨气的体积分数为25%,反应中放出a kJ热量.
将1mol N2(g)和3mol H2(g)通入一个10L的恒容密闭容器中发生反应,在不同温度下达到平衡时NH3(g)的平衡浓度如图所示.其中温度为T1时平衡混合气体中氨气的体积分数为25%,反应中放出a kJ热量.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ①③ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 达到化学平衡时,N2将完全转化为NH3 | |
| B. | 达到化学平衡时,N2、H2和NH3的物质的量浓度一定相等 | |
| C. | 达到化学平衡时,正反应和逆反应的速率都为零 | |
| D. | 达到化学平衡时,N2和H2的转化率相同且c(N2):c(H2)=1:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 实验室制备1,2-二溴乙烷的反应原理如下:
实验室制备1,2-二溴乙烷的反应原理如下:| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度g/cm3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 短周期元素X.Y.Z.W在元素周期表中的相对位置如图所示,其中w原子的最外层电子数是最内层电子数的3倍.下列判断不正确的是( )
短周期元素X.Y.Z.W在元素周期表中的相对位置如图所示,其中w原子的最外层电子数是最内层电子数的3倍.下列判断不正确的是( )| A. | x与同主族且相邻元素的气态氢化物的沸点,前者高于后者 | |
| B. | 含Y元素的盐溶液有的显酸性,有的显碱性 | |
| C. | x的气态氢化物与w的最高价氧化物的水化物反应只能生成一种盐 | |
| D. | x与H、O元素形成的化合物可以组成一种盐,其中X.H.O元素原子个数之比为2:4:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠和钾的合金可用于快中子反应堆作热交换剂 | |
| B. | 可用超纯硅制造的单晶硅来制芯片 | |
| C. | 可利用二氧化碳制造全降解塑料 | |
| D. | 氯气有毒,不能用于药物的合成 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com