
【题目】如图为我国圆明园兽首铜像—兔首和鼠首,看上去仍熠熠生辉。下列对其原因的分析最可能的是( )

A.它们表面的铜绿已用酸性溶液洗去B.利用电镀原理在其表面镀了一层耐腐蚀的黄金
C.铜的活动性很弱,与空气成分不反应D.它们是含一定比例金、银、锡、锌的铜合金
 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
①正常雨水的pH为7.0,酸雨的pH小于7.0;
②严格执行机动车尾气排放标准有利于防止大气污染;
③使用二氧化硫和某些含硫化合物增白的食品会损害人体健康;
④使用氯气对自来水消毒可能对人体有害;
⑤食品厂产生的含丰富氮、磷营养素的废水可长期排向养鱼水库
⑥人造刚玉熔点很高,可用作高级耐火材料,主要成分是Al2O3
⑦在医疗上碳酸氢钠可用于治疗胃酸过多
⑧分散系中分散质粒子的直径:Fe(OH)3悬浊液>Fe(OH)3胶体>FeCl3溶液
A.②③⑤⑥⑦⑧B.①④⑤⑥⑧
C.②③④⑥⑦⑧D.③④⑤⑦⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中错误的是( )
A.熔融状态下NaHSO4电离方程式为:NaHSO4(熔融)=Na++HSO![]() 。
。
B.强电解质的水溶液中无溶质分子,弱电解质的水溶液中有溶质分子
C.1 mol·L-1的醋酸溶液中c(H+)=0.01 mol·L-1可以证明醋酸是弱电解质
D.HF、HCl、BaSO4都是强电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于热化学反应的描述中正确的是( )
A.HCl和 NaOH 反应的中和热 H=-57.3kJ·mol-1,则H2SO4 和 Ba(OH)2反应的中和热ΔH=2×(-57.3)kJ·mol-1
B.CO(g)的燃烧热是 283.0kJ·mol-1 则 2CO2(g)=2CO(g)+O2(g)反应的ΔH=+(2×283.0 )kJ·mol-1
C.反应物的总能量低于生成物的总能量时,反应一定不能自发进行
D.一定的温度和一定的压强下,将 0.5molN2 和1.5molH2 置于密闭容器中充分反应,放热19.3kJ,热化学方程式为 N2+3H2![]() 2NH3 ΔH=-38.6kJ·mol-1
2NH3 ΔH=-38.6kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高锰酸钾常用作消毒杀菌剂、水质净化剂等。某小组用软锰矿(主要含MnO2,还含有少量SiO2、Al2O3、Fe2O3等杂质)模拟工业制高锰酸钾流程如下。试回答下列问题:

(1)配平焙烧时发生的化学反应方程式:_____MnO2+_____ ______+________O2![]() ________K2MnO4+________H2O;
________K2MnO4+________H2O;
(2)滤渣Ⅱ的成分有________(化学式);第一次通CO2不能用稀盐酸代替的原因是_______。
(3)第二次通入过量CO2生成MnO2的离子方程式为______________。
(4)将滤液Ⅲ进行一系列操作得KMnO4。由图像可知,从滤液Ⅲ得到KMnO4需经过______、________、洗涤等操作。

(5)工业上按上述流程连续生产。用含a%MnO2的软锰矿1吨,理论上最多可制KMnO4________吨。(保留2位有效数字)
(6)利用电解法可得到更纯的KMnO4。用惰性电极电解滤液Ⅱ。
①电解槽阳极反应式为________________。
②阳极还可能有气体产生,该气体是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.工业上在高温条件下用铁和氧化铝制取金属铝
B.向新制氯水中加入少量碳酸钙粉末,能增强溶液的漂白性
C.纳米铁粉可以去除被污染水体中的Pb2+、Cu2+、Hg2+,利用了其还原性
D.硫元素在自然界的存在形式有硫单质、硫化物和硫酸盐等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:pOH=-lgc(OH-)。室温下,将稀盐酸滴加到某一元碱(BOH)溶液中,测得混合溶液的pOH与离子浓度的变化关系如图所示。下列叙述错误的是

A. BOH属于弱碱
B. BOH的电离常数K=1×10-4.8
C. P点所示的溶液中:c(Cl-)>c(B+)
D. N点所示的溶液中:c(H+)=c(Cl-)+c(OH-)-c(BOH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属和非金属被广泛应用于人类生产生活中。
(1)胃液中含有盐酸,胃酸过多的人常有胃疼烧心的感觉,易吐酸水,服用含有小苏打的药品以中和过多的胃酸,其反应的离子方程式:___________________________;
(2)中华透明牙膏摩擦剂SiO2是工业制备晶体硅的原料,工业上制粗硅的反应原理是 __________;(用化学反应方程式表示)。
(3)硅酸钠的水溶液俗称水玻璃,向其中通入过量的CO2,会出现胶状沉淀,其离子方程式是_________;
(4)人体血红蛋白中含有Fe2+,若误食亚硝酸盐,会导致Fe2+转化Fe3+而中毒,服用维生素C可以解毒.对上述的分析正确的是(______)
A.亚硝酸盐是还原剂 B.维生素C是氧化剂
C.维生素C被氧化 D.亚硝酸盐发生氧化反应
(5)化学与生产、生活、社会等密切相关,下列说法正确的是(_______)
A. 二氧化硫具有漂白性,可用来增白纸浆、草帽辫、食品等
B. 酸雨是空气中二氧化碳含量超标引起的
C.工业上合成氨气可用浓氨水和生石灰混合制得
D.蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有吸水性
E.洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一,漂白粉是常用的消毒剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是某化学兴趣小组制备PCl3的实验装置(部分仪器已省略):
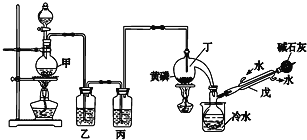
有关物质的部分性质如下:
熔点/℃ | 沸点/℃ | 其他 | |
黄磷 | 44.1 | 280.5 | 2P(过量)+3Cl2 |
PCl3 | -112 | 75.5 | 遇水生成H3PO3和HCl,遇O2生成POCl3 |
POCl3 | 2 | 105.3 | 遇水生成H3PO4和HCl,能溶于PCl3 |
请回答下列问题:
(1)仪器戊的名称为___。
(2)实验时甲中所发生反应的化学方程式为___。
(3)乙中盛放的试剂是___,其作用是___;丙中盛放的试剂是___,其作用是___。
(4)向仪器丁中通入干燥、纯净的Cl2之前,应先通入一段时间的CO2,其目的主要是___。
(5)碱石灰的作用是___(答出一条即可)。
(6)PCl3粗产品中常含有POCl3、PCl5等,加入黄磷(化学式用P表示)经加热除去PCl5的化学反应方程式为___,后通过___(填实验操作名称),即可得到PCl3纯品。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com