
某化学反应2A===B+D在四种不同条件下进行。B、D起始浓度为0,反应物A的浓度(mol·L-1)随反应时间(min)的变化情况如下表:
| 实验序号 | 温度 | 0 min | 10min | 20min | 30min | 40min | 50min | 60min |
| 1 | 800℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800℃ | c2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800℃ | c3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 820℃ | 1.0 | 0.20 | 0.20 | 0.20 | 0.20 | 0.20 | 0.20 |
根据上述数据,完成下列填空:
(1)在实验1中,反应在10至20 min时间内平均速率为________mol·L-1·min-1。
(2)在实验2中,A的初始浓度c2=______mol·L-1,反应经20 min就达到平衡,可推测实验2中还隐含的条件是____________________________。
(3)设实验3的反应速率为v3,实验1的反应速率为v1,则v3______v1(填“>”、“=”或“<”),且c3______1.0 mol·L-1(填“<”、“=”或“>”)。
(4)比较实验4和实验1,可推测该反应是________反应(填“吸热”或“放热”),理由是________________________________________________________________________
________________________________________________________________________。
(1)0.013 (2)1.0 使用了催化剂 (3)> >
(4)吸热 温度升高时,平衡向右移动
解析 (1)v(A)=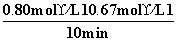
=0.013 mol·L-1·min-1
(2)对比实验1与实验2可知,反应温度相同,达平衡时的A的浓度相同,说明是同一平衡状态,即c2=1.0 mol·L-1,又因实际反应的速率快,达平衡所需时间短,说明反应中使用了催化剂。
(3)对比实验3与实验1可知,从10 min至20 min,实验1的A的浓度变化值为0.13 mol·L-1,而实验3的A的浓度变化值为0.17 mol·L-1,这说明了v3>v1。又知从0 min到10 min,A的浓度的变化值应大于0.17 mol·L-1,即c3>(0.92+0.17) mol·L-1=1.09 mol·L-1。
(4)对比实验4与实验1可知,两实验的起始浓度相同,反应温度不同,达平衡时实验4的A的浓度小,说明了实验4中A进行的程度大,即温度越高,A的转化率越大,说明正反应为吸热反应。


科目:高中化学 来源: 题型:
在下图所示的物质转化关系中(反应条件和部分生成物未全部列出),X物质可以来自于海洋中,A、B为常见气体单质,B为黄绿色气体,I、L为常见的金属单质,G为红褐色物质。请回答下列问题:

(1)X化学式为 。 (2)C化学式为 。
(3)反应①的离子方程式为 。
(4)反应②的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
反应CH3OH(l)+NH3(g)===CH3NH2(g)+H2O(g)在某温度自发向右进行,若反应的|ΔH|=17 kJ·mol-1,|ΔH-TΔS|=17 kJ·mol-1,则下列正确的是( )
A.ΔH>0,ΔH-TΔS<0 B.ΔH<0,ΔH-TΔS>0
C.ΔH>0,ΔH-TΔS>0 D.ΔH<0,ΔH-TΔS<0
查看答案和解析>>
科目:高中化学 来源: 题型:
已知反应:2NO2(g)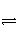
 N2O4(g)是放热反应,为了探究温度对化学平衡的影响,有人做了如下实验:把NO2和N2O4的混合气体通入甲、乙两个连通的烧瓶里,然后用夹子夹住橡皮管,把两烧瓶分别浸入两个分别盛有500 mL 6 mol·L-1的HCl溶液和盛有500 mL蒸馏水的烧杯中(两烧杯中溶液的温度相同)。
N2O4(g)是放热反应,为了探究温度对化学平衡的影响,有人做了如下实验:把NO2和N2O4的混合气体通入甲、乙两个连通的烧瓶里,然后用夹子夹住橡皮管,把两烧瓶分别浸入两个分别盛有500 mL 6 mol·L-1的HCl溶液和盛有500 mL蒸馏水的烧杯中(两烧杯中溶液的温度相同)。

(1) 该实验用两个经导管连通的烧瓶,其设计意图是
________________________________________________________________________
________________________________________________________________________。
(2) 向烧杯甲的溶液中放入125 g NaOH固体,同时向烧杯乙中放入125 g硝酸铵晶体,搅拌使之溶解。甲烧瓶内气体的颜色将____________,原因是
________________________________________________________________________
________________________________________________________________________;
乙烧瓶内气体的颜色将__________,原因是
________________________________________________________________________
________________________________________________________________________。
(3) 该实验欲得出的结论是
________________________________________________________________________
________________________________________________________________________。
(4)某同学认为该实验的设计并不完全科学,他指出此时影响化学平衡的因素不止一个,你认为他所指的另一个因素是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知反应A2(g)+2B2(g)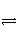
 2AB2(g) ΔH<0,下列说法正确的是( )
2AB2(g) ΔH<0,下列说法正确的是( )
A.升高温度,正反应速率增加,逆反应速率减小
B.升高温度有利于反应速率增加,从而缩短达到平衡的时间
C.达到平衡后,升高温度或增大压强都有利于该反应平衡正向移动
D.达到平衡后,降低温度或减小压强都有利于该反应平衡正向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作或叙述中不正确的是( )
A.蛋白质遇双缩脲试剂呈紫玫瑰色
B.在鸡蛋白溶液中加入浓硝酸,微热会产生黄色物质
C.用盐析法分离油脂皂化反应的产物
D.蔗糖水解时应用浓硫酸作催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
有下述有机反应类型:①消去反应 ②水解反应 ③加聚反应 ④加成反应 ⑤还原反应 ⑥氧化反应。已知CH2Cl—CH2Cl+2H2O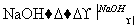 CH2OH—CH2OH+2HCl,以丙醛为原料制取1,2丙二醇,所需进行的反应类型依次是( )
CH2OH—CH2OH+2HCl,以丙醛为原料制取1,2丙二醇,所需进行的反应类型依次是( )
A.⑥④②① B.⑤①④②
C.①③②⑤ D.⑤②④①
查看答案和解析>>
科目:高中化学 来源: 题型:
通常人们把拆开1 mol某化学键所吸收的能量看成该化学键的键能。现给出化学键的键能(见下表):
| 化学键 | H—H | Cl—Cl | Cl—H |
| 键能/(kJ·mol-1) | 436 | 243 | 431 |
请计算H2(g)+Cl2(g)===2HCl(g)的反应热( )
A.862 kJ·mol-1 B.679 kJ·mol-1
C.-183 kJ·mol-1 D.183 kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com