

| 化学式 | 沉淀开始时的pH | 沉淀完全时的pH | 有关性质 |
| Co(OH)2 | 7.2 | 9.4 | Co+2HCl═CoCl2+H2↑ Co2++2NH3•H2O═Co(OH)2↓+2NH4+ Co2++2H2O?Co(OH)2+2H+ Ni+2HCl═NiCl2+H2↑ Ni2++6NH3•H2O═Ni(NH3)6]2++6H2O |
| Fe(OH)2 | 7.1 | 9.6 | |
| Fe(OH)3 | 2.3 | 3.7 | |
| Mg(OH)2 | 10.8 | 12.4 |
分析 由流程可知,钴基合金中含少量镁、镍和铁元素,加盐酸溶解后,溶液中含有Co2+、Ni2+、Fe2+、Mg2+等离子,加氨水使Ni2+转化为[Ni(NH3)6]2+,过滤分离出Co(OH)2、Mg(OH)2、Fe(OH)2,再加盐酸溶解,调节pH=4可抑制发生Co2++2H2O?Co(OH)2+2H+,再加过氧化氢,发生2Fe2++2H++H2O2=2H2O+2Fe3+,加NaF使Mg2+转化为MgF2沉淀,碳酸钠可促进Fe3+水解转化为Fe(OH)3,则滤渣为MgF2、Fe(OH)3,过滤后的滤液加浓碳酸钠反应生成CoCO3,CoCO3与盐酸、草酸铵反应生成CoC2O4•2H2O,CoC2O4•2H2O高温分解生成CoO,以此来解答.
解答 解:(1)“除镍”步骤必须控制在一定时间内完成,否则沉淀中将有部分Co(OH)2转化为Co(OH)3,此反应的化学方程式为4Co(OH)2+O2+2H2O=4Co(OH)3,故答案为:4Co(OH)2+O2+2H2O=4Co(OH)3;
(2)因Co2++2H2O?Co(OH)2+2H+,在“盐酸调pH=4”步骤中,加入盐酸的作用是防止Co2+水解,
故答案为:防止Co2+水解;
(3)“净化”步骤中加入H2O2的作用是2Fe2++2H++H2O2=2H2O+2Fe3+,由上述分析可知废渣的成分为MgF2、Fe(OH)3,
故答案为:2Fe2++2H++H2O2=2H2O+2Fe3+;MgF2、Fe(OH)3;
(4)25℃时,Ksp[Fe(OH)3]=4.0×10-38,则该温度下反应Fe3++3H2O?Fe(OH)3+3H+的平衡常数K=$\frac{{c}^{3}({H}^{+})}{c(F{e}^{3+})}$=$\frac{{c}^{3}({H}^{+}){c}^{3}(O{H}^{-})}{c(F{e}^{3+}){c}^{3}(O{H}^{-})}$=$\frac{(K{w)}^{3}}{Ksp}$=$\frac{(1{0}^{-14})^{3}}{4.0×1{0}^{-38}}$=2.5×10-5,故答案为:2.5×10-5;
(5)化合物中正负化合价的代数和为0,则CoC2O4•2H2O中C元素的化合价为$\frac{0-(-2×4)-(+2)}{2}$=+3价,在空气中高温反应的化学方程式为2CoC2O4•2H2O+O2=2CoO+4H2O+4CO2,故答案为:+3;2CoC2O4•2H2O+O2=2CoO+4H2O+4CO2.
点评 本题考查混合物分离提纯,为高考常见题型,侧重于学生的分析能力、实验能力的考查,注意把握实验的原理和目的为解答该类题目的关键,注意物质的性质及题给信息的应用,题目难度中等.


科目:高中化学 来源: 题型:推断题
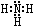 ;B分子也由Z、X两元素组成,作为运送飞船的火箭燃料,常温下是一种液态化合物.已知该化合物的相对分子质量为32,其中X元素的质量分数为12.5%,且该分子结构中只有单键.则B的结构式为
;B分子也由Z、X两元素组成,作为运送飞船的火箭燃料,常温下是一种液态化合物.已知该化合物的相对分子质量为32,其中X元素的质量分数为12.5%,且该分子结构中只有单键.则B的结构式为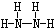 .若64g B分子与液态双氧水恰好完全反应,产生两种无毒又不污染环境的气态物质,还放出3000kJ的热量,写出该反应的热化学方程式N2H4(l)+2H2O2(l)=N2(g)+4H2O(g)△H=-1500kJ/mol.
.若64g B分子与液态双氧水恰好完全反应,产生两种无毒又不污染环境的气态物质,还放出3000kJ的热量,写出该反应的热化学方程式N2H4(l)+2H2O2(l)=N2(g)+4H2O(g)△H=-1500kJ/mol.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
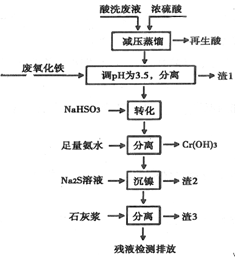
| Fe3+ | Ni2+ | Cr3+ | |
| 开始沉淀 | 1.5 | 6.7 | 4.0 |
| 沉淀完全 | 3.4 | 9.5 | 6.9 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.9mol/L | B. | 1.8mol/L | C. | 2.1mol/L | D. | 1.2mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 时间/S | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/(10-4mol/L) | 10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
| c(CO)/(10-3mol/L) | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
. .
. +
+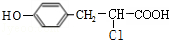 $→_{△}^{催化剂}$
$→_{△}^{催化剂}$ +HCl.
+HCl.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com