
为了得到比较纯净的物质,使用的方法恰当的是
A.向Na2CO3饱和溶液中,通入过量的CO2后,在减压、加热的条件下,蒸发得NaHCO3晶体
B.加热蒸发AlCl3饱和溶液得纯净的AlCl3晶体
C.向FeBr2溶液中加入过量的氯水,加热蒸发得FeCl3晶体
D.向FeCl3溶液里加入足量NaOH溶液,经过滤、洗涤沉淀,再充分灼烧沉淀得Fe2O3
 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案科目:高中化学 来源: 题型:
某分子式为C10H20O2的酯,在一定条件下可发生如下图的转化过程:则符合上述条件的酯的结构可能有( )
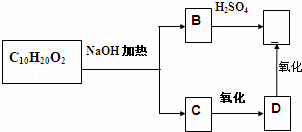
A. 2种 B. 8种 C. 6种 D. 4种
查看答案和解析>>
科目:高中化学 来源: 题型:
电解CuCl2和NaCl的混合溶液,阴极和阳极上最先分别析出的物质是()
A. H2和Cl2 B. Cu和Cl2 C. H2和O2 D. Cu和O2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中正确的是
A. 由元素的原子序数推测其在元素周期表中的位置
B. 由H-H和Cl-Cl的键长推测液氢和液氯沸点的高低
C. 由CaF2晶体中,与Ca2+距离最近的F-有8个,推知与F-距离最近的Ca2+也有8个
D. 由N-N、H-H、N-H的键能数据估算3H2(g)+N2(g)  2NH3(g)的反应热
2NH3(g)的反应热
查看答案和解析>>
科目:高中化学 来源: 题型:
废水、废气、废渣的处理是减少污染、保护环境的重要措施。
(1)烟气中的NOx必须脱除(即脱硝)后才能排放。
①列举一种由NOx引起的大气污染现象: 。
②已知:CH4 (g)+2O2(g)=CO2(g)+2H2O(l);ΔH=-890.3 kJ·mol-1
N2(g)+O2(g)=2NO(g);ΔH=+180 kJ·mol-1
则CH4脱硝的热化学方程式为CH4(g)+4NO(g)=CO2(g)+2N2(g)+2H2O(l),ΔH=_____。
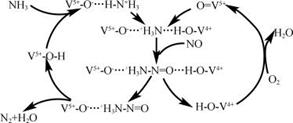
③下图是一种用NH3脱除烟气中NO的原理。该脱硝反应中,氧化剂是 ;
(2) 下图是一种三室微生物燃料电池污水净化系统原理示意图,同时处理有机废水和硝酸盐废水,并获得淡水。图中有机废水中有机物可用C6H10O5表示。
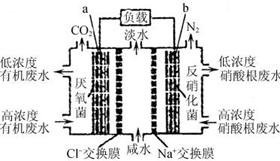
①电池正极为 。(填“a”或“b”)
②电极a上的电极反应式为 。
③电池工作过程中Na+离子移向 、Cl-离子移向 。(填“a电极”、或“b电极”)
④假设咸水中氯化钠的质量分数为2.34%,当两极总共产生7.84 L气体(标准状况下)时,理论上处理咸水 g。(忽略CO2的溶解)
查看答案和解析>>
科目:高中化学 来源: 题型:
某学生探究AgCl、Ag2S沉淀转化的原因。
| 步 骤 | 现 象 |
| Ⅰ.将NaCl与AgNO3溶液混合 | 产生白色沉淀 |
| Ⅱ.向所得固液混合物中加Na2S溶液 | 沉淀变为黑色 |
| Ⅲ.滤出黑色沉淀,加入NaCl溶液 | 较长时间后,沉淀变为乳白色 |
(1)Ⅰ中的白色沉淀是 。
(2)Ⅱ中能说明沉淀变黑的离子方程式是 ,沉淀转化的主要原因是 。
(3)滤出步骤Ⅲ中乳白色沉淀,推测含有AgCl。用浓HNO3溶解,产生红棕色气体,部分沉淀未溶解,过滤得到滤液X和白色沉淀Y。
ⅰ.向X中滴加Ba(NO3)2溶液,产生白色沉淀
ⅱ.向Y滴加KI溶液,产生黄色沉淀
①由ⅰ判断,滤液X中被检出的离子是 。
②由ⅰ、ⅱ可确认步骤Ⅲ中乳白色沉淀含有AgCl和另一种沉淀______。
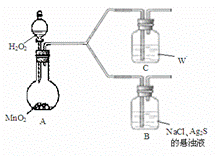
(4)该学生通过如下对照实验确认了步骤Ⅲ中乳白色沉淀产生的原因:在NaCl存在下,氧气将Ⅲ中黑色沉淀氧化。
| 现 象 | B:一段时间后,出现乳白色沉淀 |
| C:一段时间后,无明显变化 |
①A中产生的气体是_________。
②C中盛放的物质W是_________。
③该同学认为B中产生沉淀的反应如下(请补充完整):
2Ag2S + 
 +
+ 
 + 2H2O
+ 2H2O 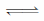 4AgCl +
4AgCl +
 + 4NaOH
+ 4NaOH
④B中NaCl的作用是_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com