
【题目】I.锰是在地壳中广泛分布的元素之一,其单质和化合物在工农业生产中有着重要的作用。已知Al的燃烧热为ΔH=—ckJ·mol—1,金属锰可用铝热法制得。其余相关热化学方程式为:3Mn3O4(s)+8Al(s)=9Mn(s)+4Al2O3(s) ΔH1 = akJ·mol—1
3MnO2(s)=Mn3O4(s)+O2(g) ΔH2 = b kJ·mol—1
则3MnO2(s)+4Al(s)=3Mn(s)+2Al2O3(s) ΔH3 =__________kJ·mol—1(用含a、b、c的式子表示)
II.无机和有机氰化物在工农业生产中应用广泛,尤其是冶金工业常用氰化物,含氰废水的处理显得尤为重要。含氰废水中的氰化物常以[Fe(CN)6]3-和CN-的形式存在,工业上有多种废水处理方法。
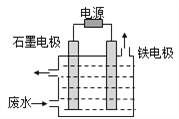
(1)电解处理法:用如图所示装置处理含CN-废水时,控制溶液pH为9~10并加入NaCl,一定条件下电解,阳极产生的ClO-将CN-氧化为无害物质而除去。铁电极为__________(填“阴极”或“阳极”),阳极产生ClO-的电极反应为__________,阳极产生的ClO-将CN-氧化为无害物质而除去的离子方程式为__________。
(2)UV(紫外光线的简称)—H2O2氧化法。
实验过程:取一定量含氰废水,调节pH,加入一定物质的量的H2O2,置于UV工艺装置中,光照一定时间后取样分析。
【查阅资料】
①在强碱性溶液中4[Fe(CN)6]3-+4OH—=4[Fe(CN)6]4-+O2↑+2H2O,[Fe(CN)6]4-更稳定;
②[Fe(CN)6]3-转化为CN-容易被H2O2除去;
③HCN是有毒的弱酸,易挥发。
①废水中的CN一经以下反应实现转化:CN—+H2O2+H2O=A+NH3↑,则A是__________(用符号表示)。
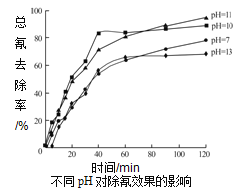
②含氰废水在不同pH下的除氰效果如图所示,pH选择的最佳范围应为__________(a.7-10;b.10-11;c.11-13),解释该pH不宜太大的原因__________。
【答案】ΔH=a/3+b — 4/3c kJ·mol-1阴极Cl-+2OH--2e-=ClO-+H2O5ClO—+2CN—+2OH—=2CO32—+N2↑+5Cl—+H2OHCO3—b碱性太强,溶液中4[Fe(CN)6]3-+4OH—===4[Fe(CN)6]4-+O2↑+2H2O生成[Fe(CN)6]4-后难以除去
【解析】I.①3Mn3O4(s)+8Al(s)=9Mn(s)+4Al2O3(s) ,②3MnO2(s)=Mn3O4(s)+O2(g),③4Al(s)+3O2(g)=2Al2O3(s) △H=-4ckJ·mol-1,(①+3×②+③)/3,得出△H=(a+3b-4c)/3kJ·mol-1; II.(1)依据电解原理,金属作阳极,先失电子,题目中提供信息:阳极产生的是ClO-,因此铁作阴极,阳极是失电子,化合价升高,控制溶液的pH在9-10,说明溶液显碱性,阳极反应式为Cl-+2OH--2e-=ClO-+H2O,ClO-将CN-氧化成无害物质,即Cl转化成Cl-,环境是碱性环境,C转化成CO32-,N转化成N2,ClO-+CN-→CO2↑+N2↑+Cl-,然后根据化合价升降进行配平,5ClO-+2CN-→2CO32-+N2↑+5Cl-,利用电荷守恒和原子守恒,配平其他,写出缺少的微粒,因此离子反应方程式为:5ClO-+2CN-+2OH-=2CO32-+N2↑+5Cl-+H2O;(2)①根据元素守恒、原子守恒、电荷守恒,A应带一个单位的负电荷,A中含有的一个C原子、一个H原子、3个氧原子,因此A为HCO3-,②根据不同pH对除氰效果的影响图,应选择除氰率最高的即pH在10~11,故选项b正确;根据查阅资料①,[Fe(CN)6]4-在碱性条件下更稳定,难以除去,具体回答是:碱性太强,溶液中4[Fe(CN)6]3-+4OH—===4[Fe(CN)6]4-+O2↑+2H2O生成[Fe(CN)6]4-后难以除去。


科目:高中化学 来源: 题型:
【题目】选择萃取剂将碘水中的碘萃取出来,这种萃取剂应具备的性质是( )
A.不溶于水,且必须易与碘发生化学反应
B.不溶于水,且比水更容易使碘溶解
C.不溶于水,且必须比水密度大
D.不溶于水,且必须比水密度小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在5-氨基四唑(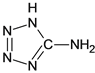 )中加入金属Ga,得到的盐是一种新型气体发生剂,常用于汽车安全气囊。
)中加入金属Ga,得到的盐是一种新型气体发生剂,常用于汽车安全气囊。
(1)基态Ga原子的电子排布式可表示为__________;
(2)5-氨基四唑中所含元素的电负性由大到小的顺序为__________;在1mol 5-氨基四唑中含有的σ键的数目为__________.
(3)叠氮酸钠(NaN3)是传统家用汽车安全气囊中使用的气体发生剂.
①叠氮酸钠(NaN3)中含有叠氮酸根离子(N3-),根据等电子体原理N3-的空间构型为__________.
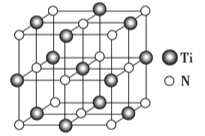
②以四氯化钛、碳化钙、叠氮酸盐作原料,可以生成碳氮化 钛化合物.其结构是用碳原子取代氮化钛晶胞(结构如图示)顶点的氮原子,这种碳氮化钛化合物的化学式为__________.
③[Ti(OH)2(H2O)4]2+中的化学键有__________.
a.σ键 b.π键 c.离子键 d.配位键.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知分解1mol KClO3放出热量38.8kJ,在MnO2下加热,KClO3的分解机理为:
①2KClO3+4MnO2![]() 2KCl+2Mn2O7 慢
2KCl+2Mn2O7 慢
②2Mn2O7![]() 4MnO2+3O2 快
4MnO2+3O2 快
下列有关说法不正确的是( )
A.1 mol KClO3所具有的总能量高于1 mol KCl所具有的总能量
B.KClO3分解速率快慢主要取决于反应①
C.1 g KClO3 ,1 g MnO2,0.1 g Mn2O7混合加热,充分反应后MnO2质量为1 g
D.将固体二氧化锰碾碎,可加快KClO3的分解速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】相同状况下,等质量的O2和CO2相比较,下列叙述正确的是
A.体积比为8︰11 B.密度之比为1︰1
C.物质的量之比为11︰8 D.原子个数之比为12︰11
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 二氧化硫可用于杀菌、消毒
B. 煤经过气化和液化等物理变化可转化为清洁能源
C. 氯气和明矾均可做自来水的消毒剂
D. 食品保鲜剂中所含铁粉和生石灰均作还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验中需用2.0molL-1的Na2CO3溶液950mL,配制时应选用容量瓶的规格和称取Na2CO3固体的质量分别为 ( )
A. 1 000mL;212.0g B. 500mL;100.7g
C. 1000mL;201.4g D. 100mL;21.2g
查看答案和解析>>
科目:高中化学 来源: 题型:
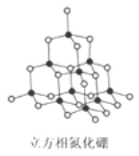
【题目】氮化硼(BN)晶体有多种相结构。六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作高温润滑剂。立方相氮化硼是超硬材料,有优异的耐磨性。它们的晶体结构如右图所示。关于这两种晶体的说法正确的是

A.两种晶体均为原子晶体
B.立方相氮化硼含有σ键和π键,所以硬度大
C.六方相氮化硼层结构与石墨相似却不导电的原因是层状结构中没有自由移动的电子
D.NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一.1mol NH4BF4含有1 mol配位键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com