
| A. | 5个 | B. | 4个 | C. | 3个 | D. | 2个 |
分析 ①根据为防止倒吸,在排水法收集满氧气后,先移出导管,后撤离酒精灯进行解答;
②根据给试管加热时要防止局部受热炸裂试管进行解答;
③稀醋酸能够中和碱液,且对桌子腐蚀性较小;
④根据可燃性气体在点燃前要验纯进行解答;
⑤测溶液的pH时,如果将试纸润湿,则会对溶液造成稀释;
解答 解:①高锰酸钾加热制备氧气实验中,为防止倒吸,在排水法收集满氧气后,先移出导管,后撤离酒精灯,故①正确;
②给试管加热时要防止局部受热炸裂试管,可以先给试管来回均匀加热,后固定局部加热,故②正确;
③碱液具有腐蚀性,而醋酸腐蚀性较小,且能够中和碱液,如果大量碱液流到桌子上,应该先用稀醋酸溶液中和,后用抹布抹去,故③正确;
④可燃性气体在点燃前要验纯,防止发生爆炸事故,故④正确;
⑤测溶液的pH时,如果将试纸润湿,则会对溶液造成稀释,会对所测的pH造成误差,故⑤错误;
故选B.
点评 本题考查学生化学是按基本操作知识,理解掌握实验的先后顺序的前提是理解反应原理,较简单.


科目:高中化学 来源: 题型:选择题
| A. | Na+、NH4+、Cl-、SO42- | B. | Fe2+、H+、SiO32-、ClO- | ||
| C. | Mg2+、K+、OH -、SO42- | D. | K+、Fe3+、NO3-、I- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 银片为正极,发生的反应为:Ag++e-=Ag | |
| B. | 进行实验时,琼脂中K+移向Mg(NO3)2溶液 | |
| C. | 取下盐桥,原电池仍可工作 | |
| D. | 在外电路中,电子从正极流向负极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③④ | B. | ①③ | C. | ②③ | D. | ①②⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .有人提出,以对甲基苯酚为原料合成PHBA的途径如下:
.有人提出,以对甲基苯酚为原料合成PHBA的途径如下: $→_{①}^{(CH_{3})SO_{4}/OH-}$
$→_{①}^{(CH_{3})SO_{4}/OH-}$ $→_{②}^{Cl_{2}/光照}$C$→_{③}^{NaOH溶液/加热}$D$\stackrel{O_{2}、Cu/加热}{→}$EPHBA
$→_{②}^{Cl_{2}/光照}$C$→_{③}^{NaOH溶液/加热}$D$\stackrel{O_{2}、Cu/加热}{→}$EPHBA
 .
. 或
或 (只写一种).
(只写一种).查看答案和解析>>
科目:高中化学 来源: 题型:填空题
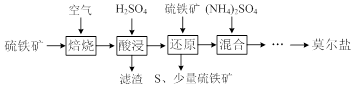
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

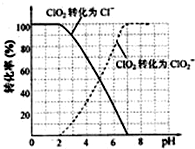
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com