
【题目】在密闭容器中进行下列反应,M(g)+N(g) ![]() R(g)+2L, 此反应符合下图所示图象。R%为R在平衡混合物中的质量分数,则该反应
R(g)+2L, 此反应符合下图所示图象。R%为R在平衡混合物中的质量分数,则该反应

A. 正反应是吸热反应,L是气体
B. 正反应是放热反应,L是气体
C. 正反应是吸热反应,L是固体
D. 正反应是放热反应,L是固体或液体
科目:高中化学 来源: 题型:
【题目】在10 L恒容密闭容器中充入X(g)和Y(g),发生反应X(g)+Y(g) ![]() M(g)+N(g),所得实验数据如下表:
M(g)+N(g),所得实验数据如下表:
实验 编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | ||
n(X) | n(Y) | n(M) | |||
① | 700 | 0.40 | 0.10 | 0.090 | |
② | 800 | 0.10 | 0.40 | 0.080 | |
③ | 800 | 0.20 | 0.30 | a | |
④ | 900 | 0.10 | 0.15 | b | |
下列说法正确的是( )
A. 实验①中,若5 min时测得n(M)=0.050 mol,则0至5 min时间内,用N表示的平均反应速率v(N)=1.0×10-2 mol·L-1·min-1
B. 实验②中,该反应的平衡常数K=2.0
C. 实验③中,达到平衡时,X的转化率为60%
D. 实验④中,达到平衡时,b>0.060
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上除去SO2尾气有多种方法.
I:烟道气中除去SO2的方法:2CO(g) + SO2(g) 2CO2(g)+ S(l)+Q (Q>0)
(1)该反应的平衡常数表达式为________。若保持其他条件不变,缩小反应容器的体积,平衡常数将会________ (选填“变大”、 “变小”或“不变”) 。
(2)下图是平衡时SO2的质量在不同温度下随压强的变化曲 线,判断: T1________T2 (选填“>”、“<”或“=”)。

(3)若在2L的密闭容器中进行上述反应,经测定在5 min内气体的质量减小了1.6g。则0~5 min的平均反应速率v(CO2)= _________________________________ 。
II:硫酸工业中用氢氧化钠溶液吸收SO2:2NaOH + SO2 → Na2SO3 + H2O, Na2SO3 + SO2 + H2O → 2NaHSO3已知: Na2SO3溶液显碱性,NaHSO3溶液显酸性,两者均易被氧化。
(1)用离子方程式解释Na2SO3溶液显碱性的原因。________________________
(2)若测得某次吸收SO2后的溶液的pH=7 (常温),则该溶液中c(H+)________ c(OH-) (选填“>”、“<”或“=”,下同),c(Na+)________ c(SO3 2-)+c(HSO3-)。上述溶液在空气中放置一段时间后,溶液的pH________7;原因是________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用纯净干燥的氯气通过如下装置与铁反应。(已知:氯气与铁的产物具有很强的吸湿性,应避免接触潮湿空气。)
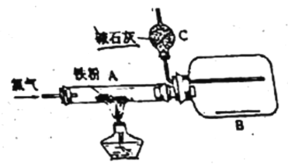
(1)当纯净干燥的氯气通过灼热铁粉时,可以看到装置A内产生_______,A中发生反应的化学方程式为:_______________。
(2)产物用氯气赶入装置B中冷却收集,推测装置C的作用是_______。
a.吸收多余的氯气 b.吸收空气中的水蒸气
c.吸收空气中的二氧化碳 d.吸收生成的氯化氢
(3)实验前需要用氯气排出装置内原有的空气,请给出一种简易判断装置内已充满氯气的方法__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于A(g)+2B(g)===3C(g)的化学反应,下列表示的反应速率最大的是
A. v(A)=0.6mol/(L·min) B. v(B)=1.2mol/(L·min)
C. v(C)=1.2mol/(L·min) D. v(B)=0.03mol/(L·s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为元素在生物体内的含量分布情况,下列表述不正确的是( )

A.I在非生物界中都能找到,体现了生物界与非生物界的统一性
B.Ⅱ含量虽少,但却是生物体正常生命活动不可缺少的
C.Ⅱ和Ⅲ称为必需元素,一旦缺乏就可能会导致相应的病症
D.P、S、K 、B、Ca、属于大量元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸橙花酯是一种食用香料,其结构简式如图所示,关于该有机物的下列叙述中正确的是
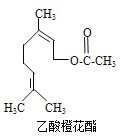
①分子式为C12H20O2
②能使酸性KMnO4溶液褪色
③能发生加成反应,但不能发生取代反应
④它的同分异构体中可能有芳香族化合物,且属于芳香族化合物的同分异构体有8种
⑤1mol该有机物水解时只能消耗1molNaOH
⑥1mol该有机物在一定条件下和H2反应,共消耗H2为3mol
A. ①②③ B. ①②⑤ C. ①②⑤⑥ D. ①②④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】配合物Fe(CO)5的熔点一20℃,沸点103℃。可用于制备纯铁。Fe(CO)5的结构如图所示。

(1)基态Fe原子的价电子排布式是_____________________;Fe(CO)5晶体类型属于__________晶体。
(2)CO分子中C、O原子都满足8电子稳定结构,CO分子的结构式是________,写出与CO互为等电子体的分子的电子式:___________________。
(3)C、O、Fe的第一电离能由大到小的顺序为_______________________。
(4)关于Fe(CO)5,下列说法正确的是______。
A. Fe(CO)5是非极性分子,CO是极性分子 B. Fe(CO)5中Fe原子以sp3杂化方式与CO成键
C.1molFe(CO)5含有10mol配位键 D.Fe(CO)5==Fe+5CO反应中没有新化学键生成
(5)铁的三种晶体的晶胞均为立方晶胞,三种晶体的晶胞如下图所示。

①上述三种晶体的晶胞中属于面心晶胞的是______(填“a”“δ””或“γ”)-Fe。
②a-Fe晶胞中铁原子的配位数为_______________。
③γ-Fe晶胞的边长为apm,则γ-Fe单质的密度为____g/cm3(NA表示阿伏伽德罗常数的值,列出计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在300mL的密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:Ni(s)+4CO(g)Ni(CO)4(g),已知该反应平衡常数与温度的关系如表:
温度/℃ | 25 | 80 | 230 |
平衡常数 | 5×104 | 2 | 1.9×10﹣5 |
下列说法不正确的是
A. 上述生成Ni(CO)4(g)的反应为放热反应
B. 25℃时反应Ni(CO)4(g)Ni(s)+4CO(g)的平衡常数为2×10﹣5
C. 80℃达到平衡时,测得n(CO)=0.3mol,则Ni(CO)4的平衡浓度为2 mol/L
D. 在80℃时,测得某时刻,Ni(CO)4、CO浓度均为0.5mol/L,则此时v(正)>v(逆)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com