
| A.磷 | B.镁 | C.铝 | D.铁 |
科目:高中化学 来源:不详 题型:单选题
| A.镁和铝与同浓度的盐酸反应铝没镁反应剧烈,所以铝比镁的金属性强 |
| B.Mg(OH)2溶液的碱性比NaOH溶液的碱性弱,所以镁比钠的金属性强 |
| C.铁能从CuSO4溶液中置换出铜,所以铁比铜的金属性强 |
| D.电解含Ag+和CU2+的溶液时,Ag+优先放电,所以银比铜的金属性强 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Na与Mg | B.Fe与Zn | C.Al与Cu | D.Mg与Zn |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.所有的金属都是固态的 |
| B.金属具有导电性、导热性和延展性 |
| C.金属原子只有还原性,其阳离子只有氧化性 |
| D.金属元素在自然界中都是以化合态存在的 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
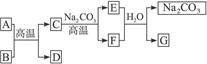
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.出水的大量瓷器为传统的硅酸盐产品 |
| B.除去瓷类器件表面污垢可以选用热烧碱溶液 |
| C.随船沉浸在海水中的铜、银等古钱币和铁制品,以铁制品被腐蚀的最厉害 |
| D.金、银、铜、铁都能溶于硝酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com