


科目:高中化学 来源:不详 题型:填空题
 、Mg2+、Fe3+、Al3+、
、Mg2+、Fe3+、Al3+、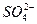 等离子,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示,由此可知,该溶液中肯定含有的阳离子是_____________,且各阳离子的物质的量之比为_____________;肯定不含有的阳离子是_____________;检验可能含有的某种阳离子的实验方法是____________________________________________________。
等离子,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示,由此可知,该溶液中肯定含有的阳离子是_____________,且各阳离子的物质的量之比为_____________;肯定不含有的阳离子是_____________;检验可能含有的某种阳离子的实验方法是____________________________________________________。
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Na+ | B.I- | C.S2- | D.Cl- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Cu,Fe3+ | B.Fe2+,Fe3+ | C.Cu,Cu2+,Fe | D.Cu,Fe2+,Fe |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 化学式 | 电离常数 |
| HClO | K=3×10-8 |
| H2CO3 | K1=3×10-3 |
| K2=3×10-11 |
| A.向Na2CO3溶液中滴加少量氯水:CO32-+2Cl2+H2O=2Cl-+2HClO+CO2 |
| B.向NaHCO3溶液中滴加少量氯水:2HCO3-+CI2=CI-+CIO-+2CO2+H2O |
| C.向NaClO溶液中通入少量CO2:CO2+NaClO+H2O=NaHCO3+HClO |
| D.向NaClO溶液通入足量CO2:CO2+2NaClO+H2O=Na2CO3+2HClO |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Fe的价层电子排布式为3d64s2 | B.35Br的电子排布式可简写为[Ar]4s24p5 |
C.NH4Cl的电子式为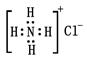 | D.氯离子结构示意图为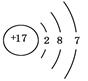 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.中子数为20的氯原子: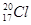 |
B.HClO的电子式: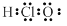 |
C.K2O的电子式: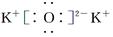 |
D.熔融状态下硫酸氢钾的电离方程式:KHSO4=K++H++SO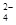 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com