
| A. | pH=7的溶液中:Na+、Fe3+、NO3-、Cl- | |
| B. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=1012的溶液中:NH4+、Mg2+、NO3-、SO42- | |
| C. | 能使甲基橙变红色的溶液中:Na+、K+、Cl-、SiO32- | |
| D. | $\frac{{K}_{W}}{c({H}^{+})}$=1×10-13mol•L-1的溶液中:Na+、NH4+、CH3COO-、HCO3- |
分析 A.铁离子在pH为4.4左右沉淀完全;
B.溶液显酸性;
C.能使甲基橙变红色的溶液,显酸性;
D.由信息可知c(OH-)=1×10-13mol•L-1,溶液显酸性.
解答 解:A.铁离子在pH为4.4左右沉淀完全,则pH=7的溶液中不能大量存在Fe3+,故A不选;
B.溶液显酸性,该组离子之间不反应,可大量共存,故B选;
C.能使甲基橙变红色的溶液,显酸性,不能大量存在SiO32-,故C不选;
D.由信息可知c(OH-)=1×10-13mol•L-1,溶液显酸性,不能大量存在CH3COO-、HCO3-,故D不选;
故选B.
点评 本题考查离子共存,为高频考点,把握习题中的信息、离子之间的反应为解答的关键,侧重分析与应用能力的考查,注意复分解反应的判断,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 制备氯气装置中的分液漏斗 | B. | 制备Fe(OH)2操作中的胶头滴管 | ||
| C. | 分馏石油时的温度计 | D. | 将氯化氢气体溶于水时的导管 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 加热聚丙烯废塑料可以得到炭、氢气、甲烷、乙烯、丙烯、苯和甲苯,用下图所示装置探究废旧塑料的再利用.下列叙述不正确的是( )
加热聚丙烯废塑料可以得到炭、氢气、甲烷、乙烯、丙烯、苯和甲苯,用下图所示装置探究废旧塑料的再利用.下列叙述不正确的是( )| A. | 乙烯分子中共用电子对数为5 | B. | 装置B的试管中可收集到苯 | ||
| C. | 装置C中的试剂可吸收烯烃 | D. | 最后收集的气体可做燃料 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 纯净物C4H8的核磁共振氢谱峰最多为4 | |
| B. | 化学式为C8H8的有机物,一定能使酸性高锰酸钾溶液褪色 | |
| C. |  的同分异构体中,可以有醇类、但没有酚类物质 的同分异构体中,可以有醇类、但没有酚类物质 | |
| D. | 1 mol 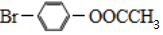 最多能与2 mol NaOH反应 最多能与2 mol NaOH反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 50mL0.1mol/L NaCl溶液 | B. | 50mL0.15mol/L MgCl2溶液 | ||
| C. | 10mL1.0mol/L FeCl3溶液 | D. | 100mL0.3mol/L KClO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:r(X)<r(Y)<r(Z)<r(W) | |
| B. | Y的最高价氧化物的水化物酸性比W的强 | |
| C. | Z的一种氧化物可能既含离子键又含共价键 | |
| D. | X、Y、W三种元素一定只能组成共价化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用食醋可除去热水壶内壁的水垢 | |
| B. | 工业上电解熔融状态的Al2O3制备Al | |
| C. | 油脂和蛋白质都是高分子化合物 | |
| D. | 利用粮食酿酒经过了淀粉→葡萄糖→乙醇的化学变化过程 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com