
【题目】下列说法不正确的是( )
A. Al箔插入稀HNO3中,无现象,说明Al箔表面被HNO3氧化,形成致密的氧化膜
B. 如图所示 ,①中为AlCl3溶液,②中为浓氨水,①中有白色沉淀生成
,①中为AlCl3溶液,②中为浓氨水,①中有白色沉淀生成
C. AlCl3![]() NaAlO2(aq)
NaAlO2(aq)![]() Al(OH)3
Al(OH)3
D. AlCl3溶液中滴加NaOH溶液后铝的存在形式:![]()
【答案】A
【解析】
A.Al与稀硝酸不发生钝化;B.浓氨水具有挥发性,挥发出的氨气属于碱性气体溶于水形成一水合氨,一水合氨和氯化铝反应生成氢氧化铝沉淀;C.氧化铝能够与氢氧化钠溶液反应生成偏铝酸钠,偏铝酸钠能够与二氧化碳气体反应生成氢氧化铝沉淀;D.氢氧化钠与氯化铝的物质的量为3:1时恰好生成氢氧化铝沉淀,当二者之比为4:1时铝离子完全转化成偏铝酸根离子。
A.Al与稀硝酸不发生钝化,与浓硝酸在常温下发生钝化,则Al箔插入稀HNO3中金属溶解,有气泡冒出,选项A错误;B.浓氨水具有挥发性,挥发出的氨气属于碱性气体溶于水形成一水合氨,一水合氨和氯化铝反应生成氢氧化铝沉淀:Al3++3NH3H2O=Al(OH)3↓+3NH4+,所以,①中有白色沉淀生成,选项B正确;C.氧化铝为两性氧化物,能够与氢氧化钠溶液反应生成偏铝酸钠,偏铝酸钠溶液能够与二氧化碳反应生成氢氧化铝沉淀,所以该转化关系能够实现,选项C正确;D.OH-与Al3+的物质的量之比为3:1时,铝元素都以Al(OH)3的形式存在,即OH-与Al3+的物质的量之比为≤3时铝元素都以Al(OH)3和Al3+的形式存在,OH-与Al3+的物质的量之比为4:1时,铝元素都以AlO2-的形式存在,即OH-与Al3+的物质的量之比为≥4时铝元素都以AlO2-的形式存在,选项D正确;答案选A。


科目:高中化学 来源: 题型:
【题目】为了使宇航员在飞船中得到一个稳定的,良好的生存环境,一般在飞船内安装盛有Na2O2或K2O2颗粒的装置,它的用途是产生氧气。下列关于Na2O2的叙述正确的是 ( )
A. Na2O2中阴、阳离子的个数比为1∶1
B. Na2O2分别与水及CO2反应产生相同量的O2时,需要水和CO2的质量相等
C. Na2O2分别与水及CO2反应产生相同量的O2时,转移电子的物质的量相等
D. Na2O2的漂白原理与SO2的漂白原理相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最早使用的化学电源是锌锰电池,即大家所熟悉的干电池(dry cell),其结构如下图所示:尽管这种电池的历史悠久,但对它的电化学过程尚未完全了解。一般认为,放电时,电池中的反应如下:

E极:2MnO2+2H2O+2e-="==" 2MnO(OH)+2OH-
F极:Zn+2NH4Cl -2e-=== Zn(NH3)2Cl2+2H+
总反应式:2MnO2+Zn+2NH4Cl ="==" 2MnO(OH)+Zn(NH3)2Cl2
下列说法正确的是
A. E极是电池的正极,发生的是氧化反应
B. F极是电池的负极,发生的是氧化反应
C. 从结构上分析,锌锰电池应属于可充电电池
D. 锌锰电池内部发生的氧化还原反应是可逆的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了探究实验室制氯气过程中反应物与生成氯气之间量的关系,设计了如下图所示的装置。

(1)装置A的名称是_____________________。
(2)该实验装置检查气密性的方法是________________________________。
(3)如果将过量二氧化锰与20mL 12mol/L的盐酸混合加热,充分反应后收集到的氯气少于0.06mol,其可能原因有__________
a.加热使浓盐酸挥发出大量HCl b.盐酸变稀后不发生该反应
c.烧瓶中残留有氯气 d.装置B中液面高于A
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物G是一种“β-兴奋剂”,其合成路线如下:

已知:


(1)写出化合物E同时符合下列条件的所有同分异构体的结构简式___________
①红外光谱显示含有三种官能团,其中无氧官能团与E相同,不含甲基
②1H—NMR谱显示分子中含有苯环,且苯环上只有一种不同化学环境的氢原子。
③苯环上只有4个取代基,能发生银镜反应
(2)下列说法不正确的是__________
A.化合物B生成C的反应为取代反应
B.1mol化合物D最多与4molH2发生加成反应
C.化合物D生成E的条件为浓氯水/铁屑
D.化合物G的分子式为C17H14Cl2NO3
(3)写出E+F→G的化学方程式________________________________________________
(4)根据题中信息,设计以苯和CH3COCl为原料制备F的合成路线(用流程图表示,其他无机试剂任选)__________________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯酸镁[Mg(ClO3)2]常用作催熟剂、除草剂等,工业大规模生产前,实验室先按如下流程进行模拟制备少量Mg(ClO3)2·6H2O:
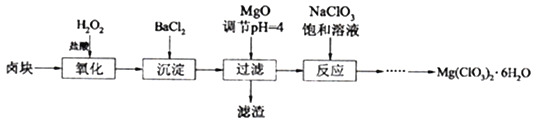
已知:①卤块主要成分为MgCl2·6H2O,含有MgSO4、FeCl2等杂质。②几种化合物的溶解度(S)随温度(T)变化曲线如右图。
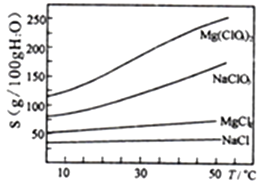
(1)卤块中加H2O2的目的是________________,写出该反应的离子方程式__________________。
(2)加入BaCl2的目的是除去SO42-,如何检验SO42-已沉淀完全?_________________。
(3)常温下,加MgO调节pH=4后溶液中c(Fe3+)=___________(已知Ksp[Fe(OH)3=4×10-38],过滤所得滤渣的主要成分有______________。
(4)加入NaClO3饱和溶液公有NaCl晶体析出,写出该反应的化学方程式:___________,请利用该反应,结合上图,制取Mg(ClO3)2·6H2O的实验步骤依次为:
①取样,加入NaClO3饱和溶液充分反应;②蒸发结晶;③___________;④冷却结晶;⑤过滤、洗涤,获得Mg(ClO3)2·6H2O晶体。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,两电极一为碳棒,一为铁片,若电流表的指针发生偏转,且a极上有大量气泡生成,则以下叙述正确的是

A. a为负极,是铁片,烧杯中的溶液为硫酸
B. b为负极,是铁片,烧杯中的溶液为硫酸铜溶液
C. a为正极,是碳棒,烧杯中的溶液为硫酸
D. b为正极,是碳棒,烧杯中的溶液为硫酸铜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质中含有两种官能团的是
A. 四氯甲烷(CCl4) B. 甘油OHCH2—OHCH2—OHOH
C. C2H5OH D. CH2=CH—CH2OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】BeCl2熔点较低,易升华,溶于醇和醚,其化学性质与AlCl3相似。由此可推测BeCl2
A.熔融态不导电B.水溶液呈中性
C.熔点比BeBr2高D.不与氢氧化钠溶液反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com