
 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源:不详 题型:填空题
 ⑥ 色,有关反应的化学方程式是 ⑦ 。
⑥ 色,有关反应的化学方程式是 ⑦ 。查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
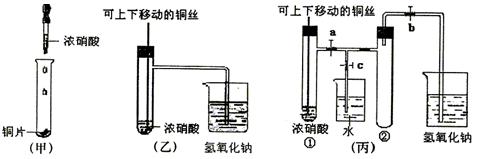



查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2NH3(g)。在一定温度下,将一定量的N2和H2通入到体积为1L的密闭容器中达到平衡后.改变下列条件,能使平衡向正反应方向移动且平衡常数不变的是__________________。
2NH3(g)。在一定温度下,将一定量的N2和H2通入到体积为1L的密闭容器中达到平衡后.改变下列条件,能使平衡向正反应方向移动且平衡常数不变的是__________________。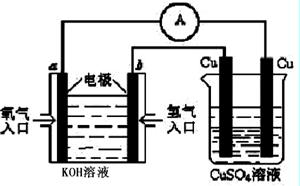
 H2(g) + CO(g) △H =" +131.3" kJ/mol
H2(g) + CO(g) △H =" +131.3" kJ/mol| A.△H >0 | B.温度较低时,△H影响为主 |
| C.△S<0 | D.温度较低时,△S影响为主 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1.0×10-3 mol | B.1.6×10-3 mol | C.2.2×10-3 mol | D.1.8×10-3 mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.它能使酚酞试液变红色 |
| B.氨水极易挥发出氨 |
| C.氨与水结合生成的一水合氨(NH3·H2O)只有小部分电离成NH4+和OH— |
| D.溶于水的氨大部分以NH3分子形式存在 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 是
是| A.Fe2+、Mg2+、Cl-、NO3-能大量共存于pH =0的溶液中 |
| B.1L浓度为l mol·L-1的NH4Cl溶液中含有NA个NH4+ |
| C.除去NO中混有的少量NO2,可将混合气体通过盛有水的洗气瓶,再用排空气法收集NO |
| D.不论是浓硝酸还是稀硝酸,与铜反应均体现出硝酸的酸性和强氧化性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com