
按要求完成下列问题
(1)甲基的电子式________ _____
(2)氢的质量分数最高的有机物的分子式
(3)相对分子质量为72且沸点最低的烷烃的结构简式
(4)1,3-丁二烯的键线式
(5)含有一个手性碳原子且式量最小的的烯烃的结构简式是:
(6)![]() 和Br2 按物质的量之比1:1发生加成反应时,可得
和Br2 按物质的量之比1:1发生加成反应时,可得
到 种产物。 和HBr按物质的量之比1:1发生加成反应时,可得到
种产物。
(7)写出和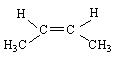 相关的异构体,各举出一例,
相关的异构体,各举出一例,
位置异构: 顺反异构: 类别异构: 。
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源: 题型:
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
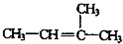 的名称是
的名称是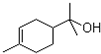 的分子式是
的分子式是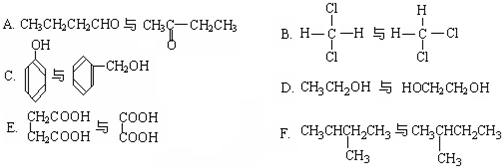
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com