
【题目】微型化学实验能有效减少污染,节约药品。下图中,某学生在衬有一张白纸的玻璃片上放置表面皿,在表面皿上的不同位置分别滴加浓度为0.1 mol/L的KBr、KI(含淀粉溶液)、NaOH(含酚酞)、FeCl2(含KSCN)溶液各1滴,在表面皿中心处放置2小粒KMnO4晶体,并滴加一滴浓盐酸,立即将表面皿盖好。可见KMnO4晶体很快溶解,并产生气体。

(1) 完成本实验中制取Cl2的化学方程式:
__KMnO4+____HCl(浓)—___KCl +_____ MnCl2 + ____ Cl2↑+__ ______ .
如该反应中消耗还原剂的物质的量为8mol,则电子转移数目为________ .
⑵b处的实验现象为___________;c处的实验现象为____________
⑶d处反应的离子方程式为_______、_______
⑷通过该实验能比较Cl2、FeCl3、KMnO4三种物质氧化性的强弱,其氧化性由强到弱的顺序是__。
【答案】2 16 2 2 5 8 H2O 8NA b处溶液变蓝色 c处溶液红色褪色 2Fe2++ Cl2 = 2Fe3++ 2Cl- Fe3++ 3SCN- = Fe(SCN)3 KMnO4 > Cl2 > FeCl3
【解析】
高锰酸钾具有强氧化性,能把盐酸氧化生成氯气,自身被还原生成氯化锰,此反应原理为2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O。在此反应中高锰酸钾是氧化剂,盐酸是还原剂,根据高锰酸钾或参加氧化还原反应的盐酸的计量数及化合价变化可判断出转移电子的数目。产物氯气具有氧化性,且易与碱反应,由此解题。
(1)高锰酸钾具有强氧化性,能把盐酸氧化生成氯气,自身被还原生成氯化锰,所以发生的反应方程式为:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O,故其配平系数为2、16、2、2、5、8H2O;该反应中氧化剂是高锰酸钾,还原剂是盐酸,根据转移电子数守恒可知,当2mol高锰酸钾参加反应时,转移电子数目=2mol×(7-2)=10mol,此时消耗还原剂的物质的量为10mol,因此当反应中消耗还原剂的物质的量为8mol,则电子转移数目为8NA;
(2)b处氯气能置换出碘,碘遇淀粉变蓝色,c处氯气能与氢氧化钠反应生成氯化钠、次氯酸钠和水,使酚酞褪色。因此b处看到的现象是溶液变蓝色,c处看到的现象是溶液红色褪去;
(3)d处 氯气氧化氯化亚铁生成氯化铁,氯化铁和硫氰化钾溶液反应使溶液呈血红色,所以d处反应的离子方程式为2Fe2++ Cl2 = 2Fe3++ 2Cl- 、 Fe3++ 3SCN-= Fe(SCN)3;
(4)2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O中氧化性KMnO4>Cl2,2FeCl2+Cl2=2FeCl3中氧化性Cl2>FeCl2,所以氧化性大小顺序是KMnO4>Cl2>FeCl3。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】用下列装置完成相关实验,合理的是( )。
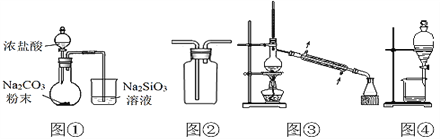
A. 图①:验证H2CO3酸性强于H2SiO3 B. 图②:收集CO2或NH3
C. 图③:分离Na2CO3溶液与CH3COOC2H5 D. 图④:分离C2H5OH与CH3COOC2H5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛及其化合物在化工、医药、材料等领域有着广泛的应用。
(1)基态钛原子的价电子排布式为_____________,与钛同周期的元素中,基态原子的未成对电子数与钛相同的有____________种。
(2)钛比钢轻、比铝硬,是一种新兴的结构材料,钛的硬度比铝大的原因是_________。
(3)在浓的TiCl3的盐酸溶液中加入乙醚,并通入HCl至饱和,可得到配位数为6、组成为TiCl3·6H2O的绿色晶体,该晶体中两种配体的物质的量之比为1:5,则该配合离子的化学式为___________。
(4)半夹心结构催化剂M能催化乙烯、丙烯、苯乙烯的聚合,其结构如下图所示。
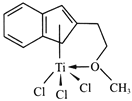
①组成M的元素中,电负性最大的是_________(填名称)。
②M中碳原子的杂化方式为____________。
③M中不含________(填代号)。
a.π键 b.σ键 c.离子键 d.配位键
(5)金红石(TiO2)是含钛的主要矿物之一。其晶胞结构(晶胞中相同位置的原子相同)如图所示。
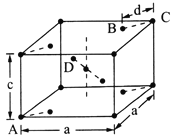
①A、B、C、D 4种微粒,其中氧原子是________(填代号)。
②若A、B、C的原子坐标分别为A(0,0,0)、B(0.69a,0.69a,c)、C(a,a,c),则D的原子坐标为D(0.19a,____,___);钛氧键的键长d=______(用代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某实验小组同学进行如图所示实验,以检验化学反应中的能量变化。
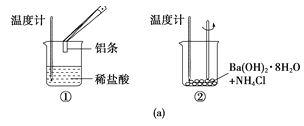
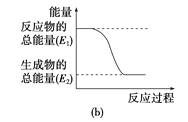
实验发现,反应后①中的温度升高,②中的温度降低。由此判断铝条与盐酸的反应是__(填“吸热”或“放热”,下同)反应,Ba(OH)2·8H2O与NH4Cl的反应是__反应。反应__(填“①”或“②”)的能量变化可用图(b)表示。
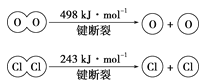
(2)已知:4HCl+O2=2Cl2+2H2O,该反应中,4molHCl被氧化,放出115.6kJ的热量,则断开1molH—O键与断开1molH—Cl键所需能量相差约为__kJ。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年诺贝尔化学奖授予了锂离子电池开发的三位科学家。一种锂离子电池的结构如图所示,电池反应式为 LixC6 + Li1-xCoO2![]() C6 + LiCoO2(x<1)。下列说法正确的是
C6 + LiCoO2(x<1)。下列说法正确的是

A.充电时 a 极接外电源的负极
B.放电时Li+在电解质中由a极向b极迁移
C.充电时若转移0.02 mol电子,石墨电极将减重0.14 g
D.该废旧电池进行“放电处理”有利于锂在LiCoO2极回收
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z、Q、R的原子序数依次增大,X的简单阴离子与锂离子具有相同的电子层结构,Y原子最外层电子数等于内层电子数的2倍,Q的单质与稀硫酸剧烈反应生成X的单质。向100mLX2R的水溶液中缓缓通入RZ2气体,溶液pH与RZ2体积关系如下图。下列说法正确的是

A.X2R溶液的浓度为0.03mol·L-1
B.工业上通常采用电解法冶炼Q的单质
C.最简单气态氢化物的稳定性:Y>Z>R
D.RZ2通入BaCl2、Ba(NO3)2溶液中,均无明显现象
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年4月,陨石坠落哥斯达黎加,再次引发了人们对“天外来客”的关注,下图中(部分产物已略去),X、Y、Z为单质,其它为化合物;E为陨石的主要成分,也是石英砂的主要成分;A为黑色磁性氧化物,请回答下列问题:

(1)写出E与焦炭在高温下反应制取Z的化学方程式,并用单线桥分析标明电子转移数目_____.
(2)写出E与 NaOH溶液反应的离子方程式 ______
(3)A与足量B的稀溶液反应生成D溶液,请用文字表述检验D中金属阳离子存在的一种实验方法:______
(4)已知在外加直流电作用下,G胶粒会向阳极区移动,这种现象叫做____;净化G胶体可采用图___(填序号)的方法,此种方法叫_____。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年诺贝尔化学奖授予约翰·古德伊纳夫、斯坦利·惠廷厄姆和吉野彰三位科学家,以表彰他们在锂电池领域所做出的巨大贡献。请回答下列问题:
(1)LiCoO2、LiFePO4常用作锂离子电池的正极材料。基态Co原子核外电子排布式为___,基态磷原子中,电子占据的最高能层符号为___;该能层能量最高的电子云在空间有___个伸展方向,原子轨道呈___形。
(2)[Co(NO3-)4]2-中Co2+的配位数为4,配体中N的杂化方式为__,该配离子中各元素的第一电离能由小到大的顺序为___(填元素符号),1mol该配离子中含σ键数目为___NA。
(3)LiFePO4属于简单磷酸盐,而直链的多磷酸盐则是一种复杂磷酸盐,如:焦磷酸钠、三磷酸钠等。焦磷酸根离子、三磷酸根离子如图所示:
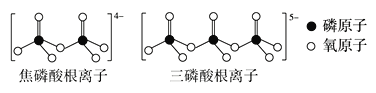
这类磷酸根离子的化学式可用通式表示为___(用n代表P原子数)。
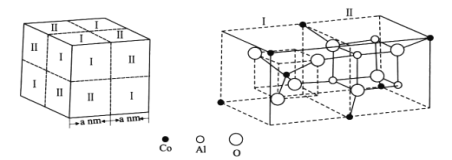
(4)钴蓝晶体结构如图,该立方晶胞由4个I型和4个Ⅱ型小立方体构成,其化学式为___,晶体中Al3+占据O2-形成的___(填“四面体空隙”或“八面体空隙”)。NA为阿伏加德罗常数的值,钴蓝晶体的密度为___g·cm-3(列计算式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素W、X、Y、Z的原子序数依次增大,W在大气中有两种同素异形体且均能支持燃烧,X的原子半径是所有短周期主族元素中最大的,非金属元素Y的原子序数是Z的最外层电子数的2倍。下列叙述不正确的是( )
A.Y、Z的氢化物稳定性Y>Z
B.Y单质的熔点高于X单质
C.X、W、Z能形成具有强氧化性的XZW
D.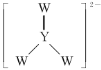 中W和Y都满足8电子稳定结构
中W和Y都满足8电子稳定结构
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com