
【题目】我国科学家研发了一种水系可逆Zn-CO2电池,将两组阴离子、阳离子复合膜反向放置分隔两室电解液,充电、放电时,复合膜层间的H2O解离成H+和OH-,工作原理如图所示。下列说法错误的是( )

A.a膜是阳离子膜,b膜是阴离子膜
B.放电时负极的电极反应式为Zn+4OH--2e-=Zn(OH)42-
C.充电时CO2在多孔Pd纳米片表面转化为甲酸
D.外电路中每通过1mol电子,复合膜层间有1mol H2O解离
【答案】C
【解析】
根据图示可知,放电时是原电池,放电时,负极为锌,锌在负极失去电子生成锌离子,结合复合膜层电离出的氢氧根离子生成Zn(OH)42-,负极的电极反应式为Zn+4OH--2e-=Zn(OH)42-,多孔Pd纳米片为正极,二氧化碳在正极得到电子转化为甲酸,电极反应为CO2+2H++2e-=HCOOH, 总的电极反应为:Zn+2OH-+2H2O+CO2= Zn(OH)42-+HCOOH,充电时的电极反应与放电时的反应相反,由此分析。
A.由图可知,a膜释放出氢离子,是阳离子膜,b膜释放出氢氧根离子,是阴离子膜,故A正确;
B.根据图示可知,放电时是原电池,负极为锌,锌在负极失去电子生成锌离子,结合复合膜层电离出的氢氧根离子生成Zn(OH)42-,负极的电极反应式为Zn+4OH--2e-=Zn(OH)42-,故B正确;
C.放电时多孔Pd纳米片为正极,二氧化碳在正极得到电子转化为甲酸,充电时是电解池,甲酸在多孔Pd纳米片表面转化为CO2,故C错误;
D.复合膜层间的H2O解离成H+和OH-,根据总的电极反应:Zn+2OH-+2H2O+CO2= Zn(OH)42-+HCOOH,锌的化合价从0价升高到+2价,外电路中每通过1mol电子,复合膜层间有1mol H2O解离,故D正确;
答案选C。


 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:高中化学 来源: 题型:
【题目】水的电离过程为H2O ![]() H+ + OH-,在不同温度下其离子积为KW(25℃)=1.0×10-14,KW(35℃)=2.1×10-14。则下列叙述正确的是
H+ + OH-,在不同温度下其离子积为KW(25℃)=1.0×10-14,KW(35℃)=2.1×10-14。则下列叙述正确的是
A.c(H+)随温度的升高而降低
B.在35℃时,c(H+)>c(OH-)
C.25℃时水的电离程度大于35℃时水的电离程度
D.水的电离是吸热的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图中A~H均为中学化学中常见的物质,A、B、H为气体,反应①是重要的工业反应,它们之间有如下转化关系(反应中生成的水已略去)。

请回答以下问题:
(1)B是________,D是________,G是________,H是________(填化学式)。
(2)工业上常利用反应①制取漂白粉,该反应的化学方程式:_____________________,漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,化学反应方程式为__________________________。
(3)A中元素的原子结构示意图为________________。
(4)上述反应中属于氧化还原反应的是_________(填写序号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法不正确的是
A. CH2=CHCOOH、CH3COOCH=CH2均可作为合成聚合物的单体
B. C6Hn分子中的六个碳原子在同一直线上,则n可能等于2
C. 2,2-二甲基丁烷与2,4-二甲基戊烷的一氯代物种类相同
D.  与
与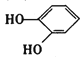 都是酚且互为同系物
都是酚且互为同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纳米级Fe3O4可用于以太阳能为热源分解水制H2,过程如下图所示。下列说法中,不正确的是
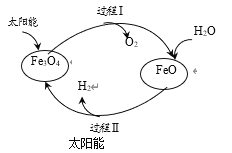
A.过程Ⅰ的反应:2Fe3O4= 6FeO+O2↑
B.过程Ⅱ的反应:2H2O =2H2↑+O2↑
C.两个转化过程都发生了氧化还原反应
D.整个过程实现了太阳能向化学能的转化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮及其化合物是重要的化工原料
(1)利用图所示装置及药品制取氨气。
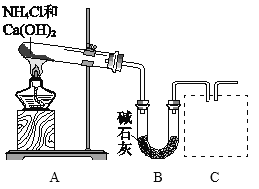
①A中制氨气的化学方程式是________。
②C处是用集气瓶收集氨气的装置,请绘出装置图。________
③证明氨气已集满的操作和现象是________。
(2)氨经催化氧化可制备硝酸,其过程中涉及如下反应。4NH3 + 5O2 ![]() 4NO + 6H2O
4NO + 6H2O
①作为氧化剂的物质是______,氮元素的化合价______(填“升高”或“降低”)。
②若反应中消耗了4 mol NH3,则生成NO的物质的量为______ mol,转移电子的物质的量为______ mol。
(3)含氮废水会加速藻类和其他浮游生物的大量繁殖,使水质恶化。利用微生物对含氮废水进行处理的流程如下:
![]()
请回答:
①过程Ⅲ发生化合反应的化学方程式为______。
②根据图1和图2,推断使用亚硝化菌的最佳条件为______。
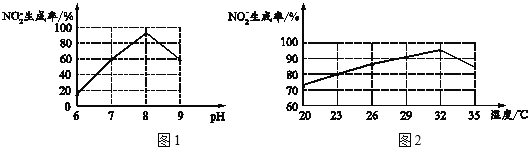
③利用微生物处理含氮废水的优点为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为氯及其化合物的“价-类”二维图。
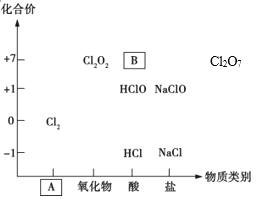
(1)填写二维图缺失的类别A_________和化学式B_________。
(2)某同学利用以下试剂研究HCl性质,进行了如下预测:
a.NaClO b.Fe c.NaOH d.KMnO4 e.AgNO3
从物质类别上看,HCl属于______,可能与__________发生反应(填序号);
从化合价角度看,Cl-具有______性,可能与_____发生反应(填序号)。
(3)某工厂用NaCl溶液制备氯气,其化学原理为如下反应:
![]() H2O +
H2O + ![]() NaCl == Cl2 +
NaCl == Cl2 + ![]() NaOH+
NaOH+![]()
①请将上述方程式补充完整,并用单线桥表示电子转移。_____________
②反应中NaCl作_________剂,理由是_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na、Fe、Cl是中学化学常见的元素。回答下列问题:
(1)含上述元素的常见化合物中,呈淡黄色的是___(填化学式)。
(2)焰色反应的实验中,Na元素的焰色为___色,观察K元素的焰色需要透过___。
(3)实验室在制备Fe(OH)2时必须隔绝空气,否则发生的现象是___。
(4)MgO与碳粉和氯气在一定条件下反应可制备MgCl2,该反应的化学方程式为___。若尾气可用足量NaOH溶液完全吸收,则生成的盐为___(写化学式,只写一种)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组为探究SO2与Fe(NO3)3稀溶液反应的情况,实验装置如图:
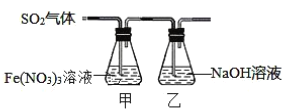
请回答:
(1)实验过程中,甲中溶液由黄色变为浅绿色但立即又变为黄色。请写出甲中溶液由浅绿色变为黄色的离子方程式___。
(2)请设计实验方案,检验反应后甲溶液中的金属阳离子___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com