
【题目】如图表示细胞内某些有机物的元素组成和功能关系,其中A、B代表元素,Ⅰ、Ⅱ、Ⅲ、Ⅳ是生物大分子,图中X、Y、Z、P分别为构成生物大分子的基本单位.请回答下列问题:
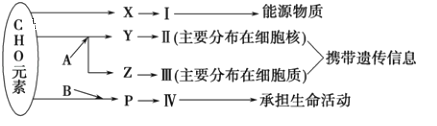
(1)图中X是_____,Ⅰ在小麦种子中主要是指_____。
(2)图中Z是_____,使用甲基绿、吡罗红混合染液染色,可使Ⅲ呈现_____色。
(3)图中P的结构通式为___________;写出由P形成Ⅳ的结构层次依次为________________________。
(4)鉴定Ⅳ时需使用双缩脲试剂,应先加_____,造成碱性环境,再加_____。(填试剂名称)
(5)分析如图中化合物的结构,回答问题。

该化合物中④表示_______。该化合物是由_____种氨基酸通过脱水缩合方式形成的,该化合物叫____________,若完全水解成为氨基酸则需要_______个水分子。
【答案】葡萄糖 淀粉 核糖核苷酸 红  氨基酸→多肽→蛋白质 NaOH(或氢氧化钠) CuSO4(或硫酸铜) 肽键 4 四肽 3
氨基酸→多肽→蛋白质 NaOH(或氢氧化钠) CuSO4(或硫酸铜) 肽键 4 四肽 3
【解析】
根据题意和图示分析可知:上图中A为N与P元素,B为氮元素、X为葡萄糖、Y为脱氧核苷酸、Z为核糖核苷酸、P为氨基酸;Ⅰ表示糖类、Ⅱ表示DNA、Ⅲ表示RNA、Ⅳ表示蛋白质。下图中①是氨基(-NH2);②、③、⑤和⑥表示R基团;④是肽键(-CO-NH-);⑦是羧基(-COOH)。据此答题。
(1)由题图知,X是由C、H、O组成的小分子物质,且被称为生命的燃料”,X是葡萄糖,Ⅰ是由葡萄糖形成的多糖,在小麦种子细胞内主要是淀粉。
(2)Ⅱ、Ⅲ的功能是携带遗传信息,二者为核酸,Z主要分布在细胞质中,故属于核糖核苷酸,使用甲基绿、吡罗红混合染液染色,可使III(核糖核酸)呈现红色。
(3)由分析可知,P为氨基酸,其结构通式为 。由P(氨基酸)形成IV(蛋白质)的结构层次为氨基酸→二肽→多肽→肽链→蛋白质。
。由P(氨基酸)形成IV(蛋白质)的结构层次为氨基酸→二肽→多肽→肽链→蛋白质。
(4)双缩脲试剂是用来检验蛋白质的,蛋白质中的肽键在碱性溶液中能与Cu2+络合成紫红色的化合物,因此鉴定Ⅳ时需使用双缩脲试剂,应先加NaOH(或氢氧化钠),造成碱性环境,再加CuSO4(或硫酸铜)。
(5)由分析可知,该化合物中④表示肽键,由题图可知,该化合物含有3个肽键,是由4个氨基酸脱水缩合失去3分子水形成的,因此该化合物叫做四肽,由于该化合物共含有3个肽键,所以若完全水解成为氨基酸则需要3个水分子。


科目:高中化学 来源: 题型:
【题目】常温下,将等体积,等物质的量浓度的NH4HCO3与NaCl溶液混合,析出部分NaHCO3晶体,过滤,所得滤液pH<7。下列关于滤液中的离子浓度关系不正确的是
A. ![]() <1.0×10-7mol/L
<1.0×10-7mol/L
B. c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)
C. c(H+)+c(NH4+)=c(OH-)+c(HCO3-)+2c(CO32-)
D. c(Cl-)>c(NH4+)>c(HCO3-)>c(CO32-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环丁基甲酸是重要的有机合成中间体,其一种合成路线如下:

回答以下问题:
(1)A属于烯烃,其结构简式为____________________。
(2)B→C的反应类型是_________________,该反应生成的与C互为同分异构体的副产物是__________________(写结构简式)。
(3)E的化学名称是___________________________。
(4)写出D生成E的化学方程式_______________________________________________。
(5)H的一种同分异构体为丙烯酸乙酯(CH2=CH—COOC2H5),写出聚丙烯酸乙酯在NaOH溶液中水解的化学方程式_________________________________________________________。
(6)写出同时满足下列条件的G的所有同分异构体__________________________________。
(写结构简式,不考虑立体异构)。
①核磁共振氢谱为3组峰; ②能使溴的四氯化碳溶液褪色;
③1mol该同分异构体与足量饱和NaHCO3反应产生88g气体。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 碘化银可用于人工降雨 B. 海水中含量最高的非金属元素是氯元素
C. 晶体硅常用于制造集成电路 D. 氧化镁可做耐高温材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2 L的密闭容器中,某化学反应2A![]() B+D在四种不同条件下进行,A、B、D都为气体,且B、D起始浓度为0,反应物A的物质的量(mol)随反应时间(min)的变化情况如下表:
B+D在四种不同条件下进行,A、B、D都为气体,且B、D起始浓度为0,反应物A的物质的量(mol)随反应时间(min)的变化情况如下表:

根据上述数据,回答以下问题:
(1)实验1中,10至30分钟时间内A的平均反应速率为________mol·L-1·min-1,达平衡时B物质的浓度为________,A的转化率为________。
(2)实验2中,隐含的反应条件可能是________。
(3)实验3中,A的起始的物质的量________(填“>”“<”或“=”)1.0 mol,实验3和实验1的起始速率v3________(填“>”“<”或“=”)v1,由实验1和实验5可确定上述反应为________(填“放热”或“吸热”) 反应,实验4中,该反应温度下其平衡常数为________。
(4)若开始时在实验2的密闭容器中充入1.0molB,1.0molD,达平衡时A物质的浓度为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于平衡常数的说法正确的是( )
A. 在平衡常数表达式中,反应物浓度用起始浓度,生成物浓度用平衡浓度
B. 在任何条件下,化学平衡常数是一个恒定值
C. 平衡常数的大小与温度、浓度、压强、催化剂等无关
D. 从平衡常数的大小可以推断一个反应进行的程度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列过程发生了加成反应的是( )
A.乙烯使酸性高锰酸钾溶液褪色B.将四氯化碳滴入溴水中,振荡后水层接近无色
C.乙烯使溴水褪色D.甲烷与氯气混合光照,黄绿色消失
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下0.1mol/L的CH3COOH溶液加水稀释过程中,下列数值一定变小的是
A. c(H+) B. c (H+) /c(CH3COOH)
C. c (H+)·c(OH-) D. c(OH-)/c (H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com