
| A. | 6 s | B. | 4 s | C. | 3 s | D. | 2 s |
分析 同一可逆反应中同一时间段内各物质的反应速率之比等于其计量数之比,所以v(NH3)=$\frac{2}{3}$v(H2)=$\frac{2}{3}$×0.6mol/(L•s)=0.4mol/(L.s),反应速率=$\frac{\frac{△n}{V}}{△t}$,据此计算反应时间.
解答 解:同一可逆反应中同一时间段内各物质的反应速率之比等于其计量数之比,所以v(NH3)=$\frac{2}{3}$v(H2)=$\frac{2}{3}$×0.6mol/(L•s)=0.4mol/(L.s),反应速率=$\frac{\frac{△n}{V}}{△t}$,所以反应时间=$\frac{\frac{△n}{V}}{v}$=$\frac{\frac{2.4mol}{2L}}{0.4mol/(L.s)}$=3s,故选C.
点评 本题考查反应速率有关计算,明确反应速率与计量数关系是解本题关键,熟悉反应速率基本公式,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
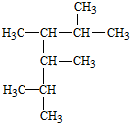 2,3,4,5-四甲基己烷
2,3,4,5-四甲基己烷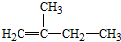 2-甲基-1-丁烯
2-甲基-1-丁烯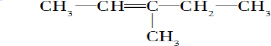 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 五氯化磷(PCl5) | B. | 次氯酸(HClO) | C. | 氯化硫(S2Cl2) | D. | 白磷(P4) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子最外层电子数:X>Y>Z | B. | 单质氧化性:X>Z>Y | ||
| C. | 离子半径:X2->Y+>Z- | D. | 原子序数:X>Y>Z |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 离子晶体中,一定不存在共价键 | B. | 原子晶体中,只存在共价键 | ||
| C. | 金属晶体的熔沸点均很高 | D. | 稀有气体的原子能形成分子晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质量相同时,跟足量的盐酸反应,在相同条件下Na2CO3产生的CO2气体多 | |
| B. | 物质的量相同时,跟足量的盐酸反应,Na2CO3所消耗H+的物质的量是NaHCO3的2倍 | |
| C. | 物质的量相同时,跟足量的盐酸反应,在相同条件下得到等体积的CO2 | |
| D. | 将它们分别加入到澄清石灰水中,都产生白色沉淀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com