
| A. | 配制0.1mol•L-1NaOH溶液过程中,将NaOH固体放在滤纸上称量 | |
| B. | 配制0.1mol•L-1的H2SO4溶液时,将量取的浓H2SO4放入容量瓶中加水稀释 | |
| C. | 配制0.1mol•L-1的NaCl溶液时,最后用胶头滴管加水至刻度线 | |
| D. | 配制0.1mol•L-1的HCl溶液时,要将量取浓盐酸的量筒和溶解用的烧杯洗涤2~3次,并将洗涤液转入容量瓶中 |
分析 A.NaOH易潮解,具有腐蚀性;
B.浓硫酸稀释放出大量的热;
C.定容时利用胶头滴管滴加;
D.量筒不需要洗涤.
解答 解:A.NaOH易潮解,具有腐蚀性,则NaOH应在小烧杯中称量,故A错误;
B.浓硫酸稀释放出大量的热,则将量取的浓H2SO4放在烧杯中稀释,冷却后转移到容量瓶中,故B错误;
C.定容时利用胶头滴管滴加,则配制0.1mol•L-1的NaCl溶液时,最后用胶头滴管加水至刻度线,操作合理,故C正确;
D.量筒不需要洗涤,将烧杯、玻璃棒洗涤2~3次,并将洗涤液转入容量瓶中,故D错误;
故选C.
点评 本题考查配制一定物质的量浓度的溶液,为基础性习题,把握实验技能、溶液配制的操作等为解答的关键,侧重分析与应用能力的考查,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 混合气体的压强 | B. | 混合气体的密度 | ||
| C. | 混合气体的平均相对分子质量 | D. | $\frac{c({N}_{2}{O}_{4})}{{c}^{2}(N{O}_{2})}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
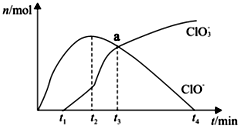 工业上将Cl 2通入冷的NaOH溶液中制得漂白液 (主要成分是NaClO ),室温下将Cl 2缓缓通入NaOH溶液中,得到ClO -、ClO 3-的物质的量与反应时间的关系如图所示,下列有关说法正确的是( )
工业上将Cl 2通入冷的NaOH溶液中制得漂白液 (主要成分是NaClO ),室温下将Cl 2缓缓通入NaOH溶液中,得到ClO -、ClO 3-的物质的量与反应时间的关系如图所示,下列有关说法正确的是( )| A. | HClO具有强氧化性,而NaClO没有氧化性 | |
| B. | 向漂白液中加入足量浓盐酸可增强漂白效果 | |
| C. | 无法求出a点时的溶液中,c( Na+ )和 c(Cl-)的比值 | |
| D. | t 2到t 4,n( ClO - )下降的原因可能是:3ClO -═2Cl-+ClO 3 - |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Zn电极上发生的反应为:2H++2e-═H2↑ | |
| B. | H+向Zn电极移动 | |
| C. | 溶液的c(H+)减小 | |
| D. | 电子由Cu转移到Zn |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 已知:反应I:4NH3(g)+6NO(g)?5N2(g)+6H2O(l)△H1
已知:反应I:4NH3(g)+6NO(g)?5N2(g)+6H2O(l)△H1| 温度/K | 反应I | 反应II | 已知: K2>K1 >K2′>K1′ |
| 298 | K1 | K2 | |
| 398 | K1′ | K2′ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 按系统命名法,化合物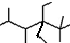 (键线式结构)的名称是2,3,5,5-四甲基-4,4-二乙基己烷 (键线式结构)的名称是2,3,5,5-四甲基-4,4-二乙基己烷 | |
| B. | 环己烯与化合物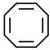 (键线式结构)互为同系物 (键线式结构)互为同系物 | |
| C. | 分子式为C4H8O2的有机物在酸性条件下可水解为酸和醇,若将所有可能得到的醇和酸重新酯化,可形成的酯共有16种 | |
| D. | 等物质的量的苯和苯甲酸完全燃烧消耗氧气的量相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 试管、蒸发皿既能用于给固体加热也能用于给溶液加热 | |
| B. | 分液漏斗既能用于某些混合物的分离也能用于组装气体发生装置 | |
| C. | 碱式滴定管既可用于中和滴定,也可用于量取一定量的NaCl或AlCl3溶液 | |
| D. | 测量酒精沸点的实验中,应使温度计水银球位于被加热的酒精中 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com