
【题目】Ⅰ.车用燃料技术的研究受到广泛关注,目前利用氢能的氢氧燃料电池技术较成熟。某兴趣小组想探究氢氧燃料电池反应的工作原理,设计如图(a)所示的实验装置。实验前,U 型管中装满溶液,电极均为铂电极。
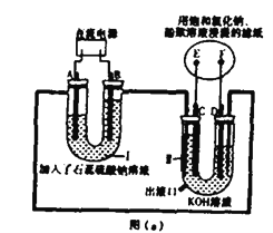
(1)I池为______(填“原电池”、“电解池”),判断A、B的电极名称的依据是:__________ B极的电极反应式:__________
(2)通电一段时间后,滤纸上发生明显颜色变化,则发生反应的化学方程式为___________
(3)Ⅱ池中电极具有导电和_______的作用,写出D的电极反应式:___________
Ⅱ.该兴趣小组查阅资料发现,现有的技术在原料氢气的储存和运输方面都存在安全隐患.2017年3月大连理工大学研究以“铂一碳化钼催化甲醇和水液化重组制备氢气”的新方法获得重大突破,并在美国《自然》杂志发表,具体原理如上图(b)所示:
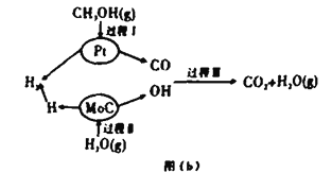
(4)过程Ⅱ属于_________(填“吸热”或“放热)过程。
(5)依据下表完成总反应的热化学方程式:____________
化学键 | C=O | H-H | C-O | H-O | C-H |
E/(kJ/mol) | 803 | 436 | 326 | 464 | 414 |
(6)天然气是一种清洁的化石燃料.也可以在一定的条件下与水反应产生CO2和H2,若生产等量氢气,则消耗甲醇和甲烷的质量比为:_________。
【答案】 电解池 因为I池实质是电解水,可观察“U”管两端生成气体的体积大小,判断产生体积大的为H2,即阴极。所以A为阴极、B极为阳极 2H2O﹣4e- ﹦O2↑+ 4 H+或4OH﹣﹣4e- ﹦O2↑﹢2H2O 2NaCl + 2H2O ![]() H2↑+ Cl2↑+ 2NaOH 催化 H2 ﹢2OH –﹣2e- ﹦2H2O 吸热 CH3OH(g)+H2O(g)═ CO2(g)+3H2(g)△H=﹢46.0 kJ·mol -1 8:3
H2↑+ Cl2↑+ 2NaOH 催化 H2 ﹢2OH –﹣2e- ﹦2H2O 吸热 CH3OH(g)+H2O(g)═ CO2(g)+3H2(g)△H=﹢46.0 kJ·mol -1 8:3
【解析】(1)根据图示,I池存在外接电源,为电解池,I池实质是电解水,可观察“U”管两端生成气体的体积大小,判断产生体积大的为H2,即阴极。所以A为阴极、B极为阳极,其中B极的电极反应式为2H2O﹣4e- ﹦O2↑+ 4 H+或4OH﹣﹣4e- ﹦O2↑﹢2H2O,故答案为:电解池;因为I池实质是电解水,可观察“U”管两端生成气体的体积大小,判断产生体积大的为H2,即阴极。所以A为阴极、B极为阳极;2H2O﹣4e- ﹦O2↑+ 4 H+或4OH﹣﹣4e- ﹦O2↑﹢2H2O;
(2)电解饱和食盐水的化学方程式为2NaCl + 2H2O ![]() H2↑+ Cl2↑+ 2NaOH,故答案为:2NaCl + 2H2O
H2↑+ Cl2↑+ 2NaOH,故答案为:2NaCl + 2H2O ![]() H2↑+ Cl2↑+ 2NaOH;
H2↑+ Cl2↑+ 2NaOH;
(3)I池生成的氢气和氧气通入Ⅱ池中形成原电池,在铂电极作催化剂时反应生成水,其中D为负极,电极反应式为H2 ﹢2OH –﹣2e- ﹦2H2O,故答案为:催化;H2 ﹢2OH –﹣2e- ﹦2H2O;
(4)根据图示,过程II为H2O(g)的催化分解,为吸热过程,故答案为:吸热;
(5)根据图示,CH3OH(g)和H2O(g)在铂一碳化钼催化作用下生成CO2(g)和H2(g)
反应的方程式为CH3OH+H2O→ CO2+3H2,根据△H=反应物的键能之和-生成物的键能之和=(414×3+326+464+2×464)kJ·mol -1-(803×2+436×3)kJ·mol -1=﹢46.0 kJ·mol -1,故答案为:CH3OH(g)+H2O(g)═ CO2(g)+3H2(g)△H=﹢46.0 kJ·mol -1;
(6)天然气是一种清洁的化石燃料.也可以在一定的条件下与水反应产生CO2和H2,反应的方程式为CH4+2H2O→CO2+4H2,CH3OH+H2O→ CO2+3H2,根据方程式可知,生产等量氢气,消耗的甲醇和甲烷的物质的量之比为![]() ,则质量之比为
,则质量之比为![]() =
=![]() ,故答案为:
,故答案为:![]() 。
。


科目:高中化学 来源: 题型:
【题目】“一酸两浸,两碱联合”法是实现粉煤灰(含SiO2、Al2O3、Fe2O3、CaO、MgO等)综合利用的新工艺。工业流程如下:

回答下列问题:
(1)聚合氯化铝铁(PAFC)化学式为[Al2(OH)nCl6-n]m·[Fe2(OH)xCl6-x]y,是一种新型高效的净水剂,PAFC中铁元素的化合价为___________。
(2)“一酸两浸”中的酸是________________(填结构式)。
(3)实际工业中“酸浸”、“碱浸”均不能充分反应,滤渣A中主要含有SiO2、Al2O3。“纯碱混合焙烧”中,它们分别发生反应的化学方程式为_____________、 ________________。
(4)“滤液B”的主要溶质有_____________(填化学式)。滤液混合后“蒸发”的作用是____________________________________。
(5)“电解”时的化学方程式________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.3 mol某烃A在氧气中完全燃烧后,生成CO2和H2O各1.2 mol。试回答:
(1)烃A的分子式为_____________。
(2)若取一定量的该烃A完全燃烧后,生成CO2和H2O各3mol,则有________g烃A参加了反应,燃烧时消耗标准状况下的氧气___________L。
(3)若烃A跟HCl反应后,生成产物中的H原子的结构环境完全相同,写出该反应的化学方程式_____。
(4)若烃A与Br2的CCl4溶液反应后的产物为1,2-二溴丁烷,请写出由烃A发生加聚反应的化学方程式_________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在氯水中存在多种分子和离子,它们在不同的反应中表现出各自的性质。下列实验现象和结论一致且正确的是( )
A. 加入有色布条,一会儿有色布条褪色,说明溶液中有Cl2存在
B. 溶液呈浅黄绿色,且有刺激性气味,说明有Cl2分子存在
C. 用盐酸酸化后,滴入AgNO3溶液产生白色沉淀,说明氯水中有Cl-存在
D. 加入NaOH溶液,氯水黄绿色消失,说明有HClO分子存在
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有X、Y、Z、W、M五种短周期元素,其中X、Y、Z、W同周期,Z、M同主族;X+与M2-具有相同的电子层结构;离子半径:Z2->W-;Y的单质晶体熔点高、硬度大,是一种重要的半导体材料。请完成下列问题:
(1)M元素的简单离子的结构示意图为_______。
(2)Z在周期表中的位置为_____,其非金属性比W的非金属性____(填“强”或“弱”)。
(3)X、Z、W的原子半径由大到小顺序为_____________(填元素符号)。
(4)Y的氢化物化学式为______,该氢化物中化学键类型为________________(填“离子键”、“极性共价键”或“非极性共价键”)。
(5)W的单质与X的最高价氧化物的水化物反应的离子方程式为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物是药物生产的中间体,其结构简式如图。下列有关叙述正确的是( )

A. 该有机物能与溴水发生加成反应
B. 该有机物与浓硫酸混合加热可发生消去反应
C. 1 mol 该有机物与足量NaOH溶液反应最多消耗3 mol NaOH
D. 该有机物经催化氧化后能发生银镜反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com